Anonymous
0
0
50 bài tập về xác định kim loại (có đáp án 2024) – Hoá học 12
- asked 6 months agoVotes
0Answers
0Views
Bài tập xác định kim loại và cách giải – Hoá học lớp 12
A. Lý thuyết trọng tâm
– Kim loại kiềm khử nước dễ dàng ở nhiệt độ thường, giải phóng khí hiđro.
Ví dụ:
Tổng quát :
2A + 2H2O → 2AOH + H2
– Từ Li đến Cs phản ứng xảy ra với nước ngày càng mãnh liệt. Natri bị nóng chảy và chạy trên mặt nước. Kali tự bùng cháy, rubiđi và xesi phản ứng mãnh liệt khi tiếp xúc với nước. Vì các kim loại kiềm dễ tác dụng với nước, với oxi trong không khí nên bảo quản, người ta ngâm chìm các kim loại kiềm trong dầu hỏa.
– Nhóm kim loại kiềm thổ: Be không khử được nước, Mg khử chậm nước khi có nhiệt độ cao, các kim loại còn lại khử mạnh nước ở nhiệt độ thường giải phóng khí H2.
Tổng quát :
M + 2H2O → M(OH)2 + H2
B. Các dạng bài
Dạng 1: Xác định một kim loại dựa vào phản ứng
1. Phương pháp giải
Bước 1: Viết phương trình phản ứng xảy ra rồi tính theo phương trình hóa học.
Ngoài ra có thể dùng phương pháp bảo toàn nguyên tố hoặc bảo toàn electron để tính nhanh số mol.
– Công thức bảo toàn electron:
nhường = nhận
– Công thức bảo toàn nguyên tố: Giả sử ta có hợp chất AxBy
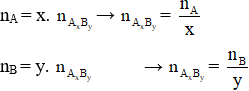
Chú ý:
Bước 2: Tính nguyên tử khối theo công thức (g/mol), từ đó suy ra tên kim loại
2. Ví dụ minh họa
Ví dụ 1:
A. Rb.
B. Li.
C. K.
D. Na.
Lời giải chi tiết
Phương trình hóa học:
Theo phương trình:
(g/mol)
Vậy M là kim loại kali (K)
Chọn C.
Ví dụ 2:
A. Na.
B. Li.
C. Rb.
D. K.
Lời giải chi tiết
Phương trình hóa học:
2X + 2H2O 2XOH + H2(1)
XOH + HCl XCl + H2O (2)
Theo phương trình (2): nXOH = nHCl = 0,103 mol
Theo phương trình (1): nX = nXOH = 0,103 mol
(g/mol)
Vậy X là kim loại kali (K)
Chọn D.
Dạng 2: Xác định hai kim loại liên tiếp trong một nhóm bằng phương pháp trung bình
1. Phương pháp giải
Bước 1: Đặt công thức chung của hai kim loại là R.
Bước 2: Viết phương trình phản ứng xảy ra rồi tính theo phương trình hóa học.
– Ngoài ra có thể dùng phương pháp bảo toàn nguyên tố hoặc bảo toàn electron để tính nhanh số mol.
Bước 3: Tính phân tử khối trung bình theo công thức , từ đó kết hợp với điều kiện của bài toán suy ra tên kim loại.
– Nếu dung dịch bazơ tạo thành sau khi phản ứng với nước được trung hòa bởi H+ thì ta có:
– Nếu dung dịch bazơ tạo thành sau khi phản ứng với nước kết tủa với các cation kim loại thì viết phương trình ion và tính.
2. Ví dụ minh họa
Ví dụ 1:
A. Li, Na.
B. Na, K.
C. K, Rb.
D. Rb, Cs.
Lời giải chi tiết
Đặt công thức chung của A và B là M
Phương trình phản ứng:
2M + 2H2O 2MOH + H2(1)
Theo phương trình:
Vậy hai kim loại là Na và K
Chọn B.
Ví dụ 2:
A. Li và Na.
B. Na và K.
C. K và Rb.
D. Rb và Cs.
Lời giải chi tiết
Đặt công thức chung của hai kim loại kiềm là R, khối lượng mol trung bình của chúng là
Chọn số mol của R tham gia phản ứng là 1 mol
Phương trình phản ứng:
2R + 2HCl 2RCl + H2 (1)
2R + H2SO4 R2SO4 + H2 (2)
Theo phương trình (1):
(3)
Theo phương trình (2):
(4)
Từ (3) và (4) ta có
Nhận xét:
X và Y là Na và K
Chọn B.
C. Bài tập tự luyện
Câu 1:
A. Na.
B. K.
C. Li.
D. Cs.
Câu 2:
A. Rb.
B. Na.
C. K.
D. Li.
Câu 3:
A. Na.
B. Ba.
C. K.
D. Ca.
Câu 4:
A. Li, Na.
B. Na, K.
C. Li, K.
D. K, Cs.
Câu 5:
A. Li, Na.
B. Na, K.
C. K, Cs.
D. Li, K.
Câu 6:
A. Na.
B. Li.
C. K.
D. Cs.
Câu 7:
A. Na2CO3.
B. Li2CO3.
C. K2CO3.
D. Cs2CO3.
Câu 8:
A. Rb và Cs.
B. Na và K.
C. Li và Na.
D. K và Rb.
Câu 9:
A. Na.
B. Ba.
C. K.
D. Ca.
Câu 10:
A. K.
B. Na.
C. Li.
D. Rb.
Câu 11:
A. Li.
B. Na.
C. K.
D. Rb.
Câu 12:
A. Li.
B. Na.
C. K.
D. Rb.
Câu 13:
A. Li, Na.
B. Na, K.
C. K, Rb.
D. Rb, Cs.
Câu 14:
A. Li và Na.
B. Na và K.
C. K và Rb.
D. Li và K.
Câu 15:
A. Li.
B. K.
C. Rb.
D. Cs.
Câu 16:
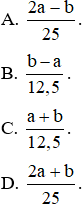
Câu 17:
A. Li2CO3 và Na2CO3; 0,03 lít.
B. Na2CO3 và K2CO3; 0,03 lít.
C. Li2CO3 và Na2CO3; 0,06 lít.
D. Na2CO3 và K2CO3; 0,06 lít.
Câu 18:
A. Li.
B. Na.
C. K.
D. Rb.
Câu 19:
A. Li và Na.
B. Na và K.
C. K và Rb.
D. Rb và Cs.
Câu 20: Cho 6,2 gam hỗn hợp 2 kim loại kiềm tác dụng hết với nước thấy có 2,24 lít H2 (đktc) bay ra. Cô cạn dung dịch thì khối lượng chất rắn khan thu được là
A. 9,4 gam.
B. 9,5 gam.
C. 9,6 gam.
D. 9,7 gam.
ĐÁP ÁN
|
Câu 1 |
Câu 2 |
Câu 3 |
Câu 4 |
Câu 5 |
Câu 6 |
Câu 7 |
Câu 8 |
Câu 9 |
Câu 10 |
|
B |
D |
A |
B |
A |
A |
A |
C |
A |
B |
|
Câu 11 |
Câu 12 |
Câu 13 |
Câu 14 |
Câu 15 |
Câu 16 |
Câu 17 |
Câu 18 |
Câu 19 |
Câu 20 |
|
A |
A |
A |
B |
B |
B |
D |
B |
B |
C |