Anonymous
0
0
50 bài tập về Tổng hợp Clo, hợp chất của Clo (có đáp án 2024) và cách giải
- asked 6 months agoVotes
0Answers
0Views
Tổng hợp Clo, hợp chất của Clo và cách giải bài tập - Hóa lớp 9
I. Lí thuyết và phương pháp giải
Để làm tốt các bài tập về clo và hợp chất của clo học sinh cần nắm vững các tính chất hóa học của clo.
1. Tính chất hóa học của clo
- Tác dụng được với hầu hết các kim loại tạo thành muối clorua
2Fe + 3Cl2 2FeCl3
- Tác dụng với khí hiđro sinh ra khí hiđro clorua
H2 (k) + Cl2 (k) 2HCl (k)
Lưu ý:
+ Khí hiđro clorua tan nhiều trong nước tạo thành dung dịch axit clohiđric.
+ Clo không phản ứng trực tiếp với oxi.
- Tác dụng với nước tạo thành nước clo
Lưu ý: Cho mẩu quỳ tím vào nước clo, lúc đầu dung dịch làm quỳ tím hóa đỏ, sau đó nhanh chóng mất màu do HClO có tác dụng tẩy màu.
- Tác dụng với dung dịch kiềm (NaOH, KOH,…)
Cl2 + 2NaOH → NaCl + NaClO + H2O
Lưu ý: Phản ứng trên là phản ứng điều chế nước Gia-ven. Nước Gia-ven cũng có tính tẩy màu như nước clo.
2. Điều chế clo
- Điều chế trong phòng thí nghiệm
MnO2 + 4HCl MnCl2 + Cl2 + 2H2O
2KMnO4 +16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
- Điều chế trong công nghiệp: Điện phân dung dịch NaCl có màng ngăn
2NaCl +2 H2O 2NaOH + Cl2 + H2
3. Hợp chất của clo hay gặp
Một số hợp chất của clo thường gặp là axit HCl, muối clorua.
II. Ví dụ minh họa
Ví dụ 1:
a. MnO2Cl2HCl Cl2 NaCl AgCl
b.
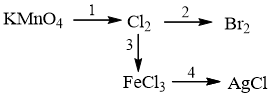
Hướng dẫn giải:
a.
(1)MnO2 + 4HCl MnCl2 + Cl2 + 2H2O
(2)Cl2 + H2 2HCl
(3)2KMnO4 +16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
(4)Cl2 + 2Na 2NaCl
(5)NaCl + AgNO3 → NaNO3 + AgCl↓
b.
(1)2KMnO4 +16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
(2)Cl2 + 2KBr → Br2 + 2KCl
(3)3Cl2 + 2Fe 2FeCl3
(4)FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl↓
Ví dụ 2:
Hướng dẫn giải:
Phương trình phản ứng hóa học:
2M + Cl2 2MCl
Bảo toàn khối lượng ta có:
Theo phương trình:
Vậy muối là NaCl.
Ví dụ 3:
Hướng dẫn giải:
Ta có: == 0,12 mol
Phương trình phản ứng hóa học:
→ VNaOH = = 0,12 lít
III. Bài tập tự luyện
Bài 1:
A. 56,83%
B. 61,2%
C. 67,5%
D. 52,98%
Bài 2:
A. 5
B. 6
C. 7
D. 8
Bài 3:
A. K
B. Na
C. Li
D. Rb
Bài 4:
A. 1,12 lít
B. 2,24 lít
C. 11,2 lít
D. 22,4 lít
Bài 5:
A. 21,3 gam
B. 20,50 gam
C. 10,55 gam
D. 10,65 gam
Bài 6:
A. 70%
B. 74,82%
C. 80,82%
D. 84,82%
Bài 7:
A. Fe
B. Na
C. Li
D. Al
Bài 8:
A. 0,1 lít
B. 0,15 lít
C. 0,2 lít
D. 0,25 lít
Bài 9:
A. 30,8g
B. 29,25g
C. 58,5g
D. 43,
Bài 10: Hàng năm trên thế giới cần tiêu thụ khoảng 45 triệu tấn khí clo. Nếu dùng NaCl để điều chế clo thì khối lượng NaCl cần dùng là (hiệu suất 100%)
A. 70,15 triệu tấn
B. 74,15 triệu tấn
C. 75,15 triệu tấn
D. 80,15 triệu tấn
Bài 11:
A. 21,2g và 10g
B. 15,9g và 15,3g
C. 18g và 13,2g
D. 16,2g và 15g
Bài 12:
A. 0,8
B.
C. 0,5
D. 1,2
Bài 13:
A. 497g
B. 511g
C. 365g
D. 438g
Bài 14:
A. 15
B. 20
C. 25
D. 10gam
Bài 15:
A.
B. 0,25
C. 0,3
D. 0,
Đáp án minh họa
|
1D |
2B |
3B |
4A |
5A |
6D |
7D |
8C |
9D |
10B |
|
11A |
12A |
13B |
14D |
15A |