Anonymous
0
0
Giải SBT Hóa 11Bài 37: Nguồn hidrocacbon thiên nhiên
- asked 6 months agoVotes
0Answers
0Views
Mục lục Giải SBT Hóa 11 Bài 37: Nguồn hidrocacbon thiên nhiên
Bài 37.1 trang 57 sbt Hóa 11: Nhận xét nào sau đây về thành phần của dầu mỏ là đúng?
A. Dầu mỏ là một hiđrocacbon ở thể lỏng.
B. Dầu mỏ là một hỗn hợp của nhiều hiđrocacbon thể lỏng.
C. Dầu mỏ là một hỗn hợp của nhiều hiđrocacbon ở thể lỏng, thể khí và thể rắn.
Lời giải:
Đáp án D
Bài 37.2 trang 57 sbt Hóa 11: Hãy ghép mỗi công đoạn của việc chế biến dầu mỏ (xử lý sơ bộ, chưng cất, crăckinh, rifominh) với nội dung cho phù hợp
Lời giải:
Đáp án
1 – C
2 – D
3 – A
4 – B
Bài 37.3 trang 58 sbt Hóa 11: Hãy ghép tên khí với nguồn khí cho phù hợp.
|
Thu được khi nung than mỡ trong điều kiện không có không khí | |||
Lời giải:
Đáp án
1 – C
2 – D
3 – B
4 – A
Bài 37.4 trang 58 sbt Hóa 11: Khi chưng cất một loại dầu mỏ, 15% (khối lượng) dầu mỏ chuyển thành xăng và 60% khối lượng chuyển thành mazut. Đem crăckinh mazut đó thì 50% (khối lượng) mazut chuyển thành xăng. Hỏi từ 500 tấn dầu mỏ đó qua hai giai đoạn chế biến, có thể thu được bao nhiêu tấn xăng?
Lời giải:
Khối lượng xăng thu được nhờ chưng cất:
tấn
Khối lượng mazut là: tấn
Khối lượng xăng thu được nhờ crăckinh là:
tấn
Khối lượng xăng thu được tổng cộng là: 150 + 75 = 225 (tấn).
Bài 37.5 trang 58 sbt Hóa 11: Một loại khí thiên nhiên có thành phần về thể tích như sau:
85% CH4; 10% C2H6; 3% N2; 2% CO2.
Lời giải:
1. Trong 1000 m3 khí thiên nhiên có 850 m3 CH4
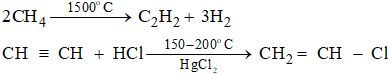
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
![]() Kg
Kg
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
![]() Kg
Kg
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20oC lên 100oC:
100.4,18(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là:
Đặt số mol C2H6 tà x thì số mol CH4 là 85.10−1x.
Ta có 1560x + 88085.10−1x = 41800
Suy ra x = 462.10−2
Thể tích khí thiên nhiên cần dùng:
![]() KJ
KJ
Bài 37.6 trang 58 sbt Hóa 11: Khi crăckinh butan, đã xảy ra các phản ứng:
Một phần butan không tham gia các phản ứng.
1. Tính phần trăm thể tích butan đã tham gia các phản ứng.
Lời giải:
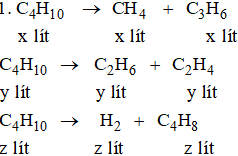
Đặt thể tích C4H10 không tham gia phản ứng là t lít.
2x + 2y + 2z + t = 47 (1)
Khi đi qua nước brom dư thì C3H6, C2H4 và C4H8 bị hấp thụ; thể tích các khí còn lại: x + y + z + t = 25 (2)
Lấy (1) - (2) ta có x + y + z = 22; đó chính là thể tích C4H10 đã phản ứng,
còn x + y + z + t = 25 cũng chính là thể tích C4H10 trước phản ứng.
Phần trăm theo thể tích của C4H10 phản ứng:
2. Giả sử đốt 25 lít khí còn lại sau khi qua nước brom
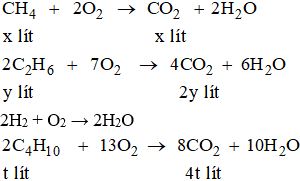
Thể tích CO2 thu được sẽ là:
x + 2y + 4t = 47 (3)
Ngoài ra theo đầu bài y = 3x (4)
Giải hệ (1), (2), (3), (4) ta được x = 5; y =15; z = 2; t = 3.
Thành phần phần trăm về thể tích của hỗn hợp A: