Anonymous
0
0
Sách bài tập Hóa học 10 Bài 22 (Kết nối tri thức): Hydrogen halide. Muối halid
- asked 6 months agoVotes
0Answers
0Views
Giải sách bài tập Hóa học 10 Bài 22. Hydrogen halide. Muối halid
Nhận biết
Bài 22.1 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Ở trạng thái lỏng, giữa các phân tử HF tạo được liên kết hydrogen mạnh.
Bài 22.2 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Vì HF tạo được liên kết hydrogen giữa các phân tử nên có nhiệt độ sôi cao bất thường so với các hydrogen halide còn lại.
Bài 22.3 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: B
Vì bán kính nguyên tử tăng dần từ F đến I, nên độ dài liên kết H-X tăng dần, năng lượng liên kết giảm dần hay độ bền liên kết giảm dần.
Bài 22.4 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: A
Độ bền liên kết H-F là lớn nhất, vì vậy nguyên tử H khó bị phân li nhất nên tính acid của dung dịch HF là mạnh nhất.
Bài 22.5 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: B
AgNO3 + NaBr → AgBr↓ (vàng nhạt) + NaNO3
Lưu ý: AgF tan, AgCl kết tủa trắng, AgBr kết tủa vàng nhạt, AgI kết tủa vàng đậm.
Bài 22.6 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: D
Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2
Bài 22.7 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: D
Hydrohalic acid thường được dùng để đánh sạch bề mặt kim loại trước khi sơn, hàn, mạ điện là HCl.
Lời giải
Đáp án đúng là: A
Hydrohalic acid được dùng làm nguyên liệu để sản xuất hợp chất chống dính teflon là HF.
Bài 22.9 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Dung dịch AgNO3 có thể phân biệt được các ion F-, Cl-, Br-, I- trong dung dịch muối
Hiện tượng: AgF tan, AgCl kết tủa trắng, AgI kết tủa vàng nhạt, AgCl kết tủa vàng đậm.
Bài 22.10 trang 68 SBT Hóa học 10:
Lời giải
Đáp án đúng là: B
KBr thể hiện tính khử khi đun nóng với dung dịch H2SO4 đặc.
2KBr + 3H2SO4 đặc → 2KHSO4 + Br2 + SO2 + 2H2O
Thông hiểu
Bài 22.11 trang 69 SBT Hóa học 10:
A. Tương tác van der Waals tăng dần.
D. Độ phân cực liên kết giảm dần.
Lời giải
Đáp án đúng là: A
Trong dãy hydrogen halide, từ HCl đến HI, nhiệt độ sôi tăng dần chủ yếu do tương tác van der Waals tăng dần.
Bài 22.12 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Trong dãy hydrogen halide, độ âm điện giảm dần từ F đến I dẫn đến độ phân cực của liên kết H-X giảm dần từ HF đến HI.
Bài 22.13 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: D
Hydrochloric acid đặc thể hiện tính khử khi tác dụng với MnO2
Bài 22.14 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: B
Hydrochloric acid loãng thể hiện tính oxi hóa khi tác dụng với kim loại
Bài 22.15 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Dung dịch HCl làm quỳ tím hóa đỏ. Dung dịch NaCl không làm quỳ tím đổi màu.
Bài 22.16 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: A
Dung dịch HF có khả năng ăn mòn thủy tinh là do xảy ra phản ứng hóa học:
SiO2 + 4HF → SiF4 + 2H2O
Bài 22.17 trang 69 SBT Hóa học 10:
A. tương tác van der Waals tăng dần.
B. độ phân cực liên kết giảm dần
Lời giải
Đáp án đúng là: D
Trong dãy hydrohalic acid, từ HF đến HI độ bền liên kết giảm dần ⇒ khả năng phân li H+ trong dung dịch tăng dần ⇒ Tính acid tăng dần.
Bài 22.18 trang 69 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
NaCl tác dụng với H2SO4 đặc chỉ xảy ra phản ứng trao đổi.
2NaCl + H2SO4 → Na2SO4 + 2HCl
Bài 22.19 trang 70 SBT Hóa học 10:
A. Dung dịch hydrofluoric acid có khả năng ăn mòn thủy tinh.
B. NaCl rắn tác dụng với H2SO4 đặc, nóng, thu được hydrogen chloride.
C. Hydrogen chloride tan nhiều trong nước.
D. Lực acid trong dãy hydrohalic acid giảm dần từ HF đến HI.
Lời giải
Đáp án đúng là: D
Trong dãy hydrohalic acid, từ HF đến HI độ bền liên kết giảm dần ⇒ khả năng phân li H+ trong dung dịch tăng dần ⇒ Tính acid tăng dần.
Bài 22.20 trang 70 SBT Hóa học 10:
Lời giải
Đáp án đúng là: C
Dung dịch AgNO3 có thể phân biệt hai dung dịch NaF và NaCl.
AgNO3 + NaF không phản ứng
AgNO3 + NaCl → AgCl (↓ trắng) + NaNO3
Vận dụng
Bài 22.21 trang 70 SBT Hóa học 10:
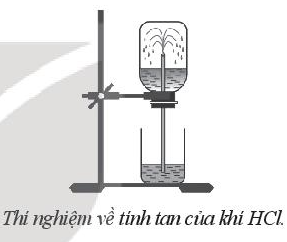
Bước 2: nhúng ống thủy tinh vào cốc nước, thấy nước phun vào bình (xem hình bên).
b) Sự biến đổi áp suất như vậy đã chứng tỏ tính chất gì của khí HCl?
Lời giải
a) Hiện tượng nước phun vào bình chứng tỏ áp suất khí trong bình đã giảm rất nhanh.
b) Sự giảm nhanh áp suất chứng tỏ khí hydrogen chloride đã tan nhanh vào nước.
Bài 22.22 trang 70 SBT Hóa học 10:
Lời giải
a) Phản ứng minh họa tác dụng của thuốc chữa đau dạ dày:
NaHCO3 + HCl → NaCl + CO2 + H2O
b) Phương trình hóa học của phản ứng thủy phân tinh bột trong môi trường acid (HCl)
(C6H10O5)n + nH2O nC6H12O6
Bài 22.23 trang 70 SBT Hóa học 10:
Lời giải
- Cho vài giọt dung dịch AgNO3 vào ống thứ nhất, thu được kết tủa màu vàng nhạt xảy ra phản ứng:
NaBr + AgNO3 → NaNO3 + AgBr↓ (màu vàng nhạt)
- Nhỏ vài giọt nước Cl2 vào ống thứ hai, lắc nhẹ xảy ra phản ứng:
2NaBr + Cl2 → 2NaCl + Br2
- Br2 tan vào trong benzene làm xuất hiện màu da cam.
Bài 22.24 trang 71 SBT Hóa học 10:
Một số kết quả thí nghiệm được ghi lại ở bảng sau.
Chất thử |
Thuốc thử |
Hiện tượng |
Các dung dịch ban đầu được kí hiệu tương ứng là
Lời giải
Đáp án đúng là: A
X làm hồ tinh bột chuyển sang màu xanh tím nên X là dung dịch iodine.
Z tác dụng với NaHCO3 tạo bọt khí nên Z là hydrochloric acid:
NaHCO3 + HCl → NaCl + CO2↑ + H2O
Còn lại Y là sodium chloride.