Anonymous
0
0
TOP 40 câu Trắc nghiệm Luyện tập: Ankin (có đáp án 2023) - Hóa 11
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa học lớp 11 Bài 33: Luyện tập: Ankin
Bài giảng Hóa học lớp 11 Bài 33: Luyện tập: Ankin
Câu 1:
A. 2.
B. 4.
C. 3.
D. 1.
Đáp án: C
Giải thích:
Có 3 công thức thỏa mãn :
CH≡C – CH2 – CH2 – CH3
CH3 – C≡C – CH2 – CH3
CH≡C – CH(CH3) – CH3
Câu 2:
A. Stiren
B. Đimetyl axetilen
C. But-1-in
D. But-1,3-dien
Đáp án: C
Giải thích: But – 1 – in: CH≡C –CH2 – CH3 có liên kết ba đầu mạch nên có phản ứng tạo kết tủa với AgNO3/NH3
Câu 3:
A. 2-metylbut-3-in
B. 3-metylbut-1-in
C. 2-metylbuta-1,3-dien
D. pent-1-in
Đáp án: B
Giải thích:
X phản ứng với AgNO3/NH3 → có nối 3 đầu mạch
→ X là CH≡C-CH(CH3)2 (3-metylbut-1-in)
Câu 4:
A. 2.
B. 3.
C. 4.
D. 1.
Đáp án: A
Giải thích:
X thể khí → số C ≤ 4
Mà
Vì X phản ứng được với AgNO3/NH3
→ có liên kết 3 đầu mạch
→ có 2 công thức cấu tạo thỏa mãn: C2H2 ; C4H4 (CH≡C – CH=CH2)
Câu 5:
A. 48,24
B. 33,84
C.14,4
D.19,44
Đáp án: B
Giải thích:
C2H2 + H2O CH3CHO
C2H2 Ag2C2 ↓
CH3CHO 2Ag ↓
Câu 6:
A. 53,85%.
B. 46,15%.
C. 50,15%.
D. 49,85%.
Đáp án: B
Giải thích:
Chỉ có C2H2 phản ứng tạo Ag2C2
Câu 7:
A. 26,88 lit
B. 44,8 lit
C. 33,6 lit
D. 22,4 lit
Đáp án: C
Giải thích:
M hh khí thoát ra = 6.2 = 16
→ Hỗn hợp khí thoát ra gồm: C2H6 và H2 dư
BTKL: mX = mY = m hh khí thoát ra + m bình Brom tăng
→ mX = mY = 0,2.8.2 + 10,8 = 14 gam
Đặt số mol C2H2 và H2 là x mol
→ mX = 26x + 2x = 14 → x = 0,5 mol
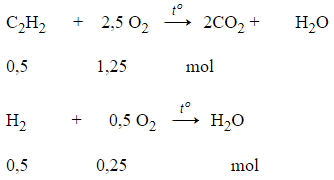
lít
Câu 8:
A. 60%
B. 50%
C. 40%
D. 80%.
Đáp án: A
Giải thích:
Xét 1 mol CH4
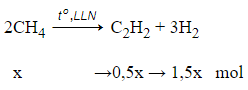
→ Sau phản ứng :
nhh = 1-x + 0,5x + 1,5x = 1 + x (mol)
Bảo toàn khối lượng :
mtrước = msau
→ 16.1 = 5.2.(1 + x)
→ x = 0,6 mol
→ H = 60%
Câu 9:
A. 0,16.
B. 0,18.
C. 0,10.
D. 0,12.
Đáp án: C
Giải thích:
a mol kết tủa là số mol của ankin còn lại.
Số mol khí giảm là số mol H2 đã phản ứng:
Bảo toàn liên kết π ta có:
→ 2.0,15 + 2.0,1 – (0,35-a)
= 2a + 0,05 → a = 0,1 mol
Câu 10:
A. axetien, but - 1 - in
B. axetilen, propin
C. propin, but - 1 - in
D. propin, but - 2 - in
Đáp án: D
Giải thích:
Số C trung bình 2 ankin =
Vì Trong X có 1 ankin không phản ứng với AgNO3
Dựa vào đáp án → Chỉ có đáp án D thỏa mãn vì but – 2 – in không phản ứng với AgNO3
Câu 11:
A. C2H2
B. C5H8
C. C4H6
D. C3H4
Đáp án: B
Giải thích:
Công thức ankin là CnH2n-2 (n ≥ 2)
→ n = 5
Vậy X là C5H8
Câu 12:
A. 180
B. 120
C. 100
D.60
Đáp án: B
Giải thích:
Gọi số mol ankan là a, anken là b, ankin là c
→ a + b + c = 0,1
Mà
→ b + 2c
= a+ b+ c + c – a
= 0,1 + 0,02 = 0,12 mol
→ 0,12.160 = 19,2 gam.
→ m = 120g
Câu 13:
A. 11,2
B. 13,44
C. 5,60
D. 8,96
Đáp án: A
Giải thích:
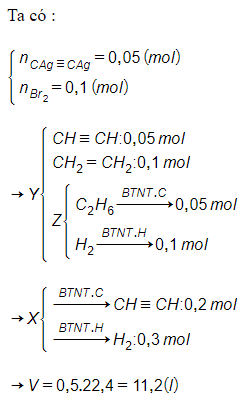
Câu 14:
A. C2H2.
B. C2H4.
C. C4H6.
D. C3H4.
Đáp án: A
Giải thích:
→ Y chứa ankan
Ta có: nY = 0,3 – 0,2 = 0,1 mol
→ số C = 2
Vậy công thức phân tử của Y: C2H6
Vì áp suất trong bình trước khi nung nóng gấp 3 lần áp suất trong bình sau khi nung ở cùng điều kiện nhiệt độ
→ nhỗn hợp trước = 3n hỗn hợp sau
→ X là ankin C2H2
Câu 15:
A. 33,6 lít.
B. 22,4 lít.
C. 16,8 lít.
D. 44,8 lít.
Đáp án: A
Giải thích:
Y gồm 4 chất :
C2H2(dư) ; C2H4 ; C2H6 ; H2
m bình tăng =
→ Khí thoát ra là C2H6 và H2
mZ = M.n = 8.2.0,2 = 3,2 g
Bảo toàn khối lượng:
Mà
→ x = 0,5
thể tích O2 cần để đốt cháy hỗn hợp Y = thể tích O2 cần để đốt cháy hỗn hợp X
lít
Câu 16:
A. 19,2 gam.
B. 1,92 gam.
C. 3,84 gam.
D. 38,4 gam.
Đáp án: A
Giải thích:
Đặt nankan = x
→ nanken = x, n ankin = 2x
→ n hỗn hợp X = x + x + 2x = 0,8 mol
→ x = 0,2
ankin là C2H2
Gọi CTPT của ankan, anken lần lượt CnH2n+2 ; CmH2m
→ hỗn hợp X có 0,2 mol CH4 ; 0,2 mol C2H4 và 0,4 mol C2H2→ m hỗn hợp = 19,2 g
Câu 17:
A. C3H4 và 10%.
B. C3H4 và 90%.
C. C3H8 và 20%.
D. C4H6 và 30%.
Đáp án: A
Giải thích:
Ta có
Tỉ lệ % theo thể tích = tỉ lệ số mol
Giả sử
nC : nH = 3 : 4 → CTĐGN: (C3H4)n
Mà hidrocacbon ở thể khí nên n = 1 → C3H4
BTNT oxi :
Câu 18:
A. C2H4.
B. CH4.
C. C2H6.
D. C3H8.
Đáp án: C
Giải thích:
Ta có:
Hiđrocacbon X cũng có 2C.
Hiđrocacbon X có số H lớn hơn 4
→ có số H = 6
→ X là C2H6
Câu 19:
A. 25
B. 20
C. 34
D. 24
Đáp án: B
Giải thích:
∑nπ bđ = 0,14.2 + 0,1.3 = 0,58 mol
→ n lk π sau pư hidro hóa = 0,58 – 0,2 = 0,38 mol
nhh khí có lk 3 đầu mạch bị giữ lại :
0,14 + 0,1 – nZ = 0,1 mol (I)
n lk π trong hh Z = 0,12 mol (II)
→ Số mol π đã biết
= 2.n π(I) + nπ(II) = 0,32 mol ≠ n π thực tế = 0,38 mol
→ Trong 2 hợp chất bị AgNO3/ NH3 giữ lại chứa CH≡C – CH = CH2 dư
dư = 0,38 – 0,32 = 0,06 mol
Vì ∑n khí có liên kết ba = 0,1 mol → khí còn lại phải là C2H2 : 0,04 mol (Nếu là C4H6 thì Y không thể chứa tới 7 HC)
→ m↓ =
= 0,04. 240 + 0,06. 159
=19,14 g ≈ 20 g
Câu 20:
A. 3
B. 4
C. 5
D. 6
Đáp án: B
Giải thích:
CH≡C-CH2-CH2-CH2-CH3
CH≡C-CH2-CH(CH3)-CH3
CH≡C-CH(CH3)-CH2-CH3
CH≡C-C(CH3)3
Vậy có 4 đồng phân thỏa mãn đề bài.
Câu 21:
A. 16.
B. 0.
C. 24.
D. 8.
Đáp án: C
Giải thích:
BTKL: ns.Ms = nđ.Mđ
→ 0,6.2 + 0,15.52 = ns.20
→ ns = 0,45 mol
Số mol khí sau phản ứng giảm là số mol H2 phản ứng:
= nđ – ns = 0,75 – 0,45 = 0,3 mol
BT liên kết π ta có:
n π đầu – n π pư = n π sau
hay 3nvinylaxetilen – pư =
→ pư = 3.0,15 – 0,3 = 0,15 mol
→ = 0,15.160 = 24 gam
Câu 22:
A. C2H2
B. C3H4
C. C4H6
D. C4H8
Đáp án: A
Giải thích:
Chọn số mol hỗn hợp X là 1 mol (nX = 1 mol)
→ mX = 6,8 (g)
BTKL mX = mY = 6,8 (g)
→ nY = = 0,6 mol
= nX - nY = 1 - 0,6 = 0,4 mol
Vì hỗn hợp Y không làm mất màu nước Br2 nên trong Y chỉ có ankan.
![]()
Theo phương trình mol ankin = mol H2 phản ứng = 0,2 mol
mX = (14n – 2).0,2 + 2(1 - 0,2) = 6,8
→ n = 2. CTPT: C2H2.
Câu 23
A. C2H2; 8,5g
B. C3H4; 8,5g
C. C4H6; 8,75g
D. C5H8; 8,75g
Đáp án: D
Giải thích:
Do A tác dụng được với AgNO3 trong NH3 nên A là ank-1-in:
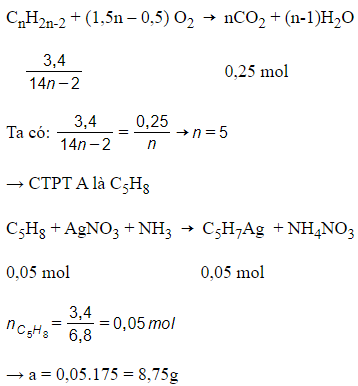
Câu 24: Hỗn hợp ban đầu gồm 1 ankin, 1 anken, 1 ankan và H2 với áp suất 4 atm. Đun nóng bình với Ni xúc tác để thực hiện phản ứng cộng sau đó đưa bình về nhiệt độ ban đầu được hỗn hợp Y, áp suất hỗn hợp Y là 3 atm. Tỉ khối hỗn hợp X và Y so với H2 lần lượt là 24 và x. Giá trị của x là
A. 18.
B. 34.
C. 24.
D. 32.
Đáp án: D
Giải thích:
Do nhiệt độ và thể tích bình không thay đổi
Giả sử nX = 4 → nY = 3
mX = 4.24.2 = 192 = mY
→ MY = = 64
→ x = 32
Câu 25: Hỗn hợp A gồm H2, C3H8, C3H4. Cho từ từ 12 lít A qua bột Ni xúc tác. Sau phản ứng được 6 lít khí duy nhất (các khí đo ở cùng điều kiện). Ti khối hơi của A so với H2 là
A. 11.
B. 22.
C. 26.
D. 13.
Đáp án: A
Giải thích:
Khí duy nhất là C3H8.
BTKL: mđ = ms
→ nđ.Mđ = ns.Ms
→ Mđ =
= 22
= 11
Câu 26:
A. 17,2.
B. 9,6.
C. 7,2.
D. 3,1.
Đáp án: D
Giải thích:
Bảo toàn khối lượng
→ m hỗn hợp X = m hỗn hợp Y
= m bình tăng + m hỗn hợp khí thoát ra
m hỗn hợp X = m bình tăng + m hỗn hợp khí thoát ra
0,1.40 + 0,2.28 + 0,35.2 = m bình tăng + 0,3.12.2
→ m bình tăng = 3,1 g
Câu 27:
A. 14,4.
B. 10,8.
C. 12.
D. 56,8.
Đáp án: C
Giải thích:
m hidrocacbon = mC + mH
= = 12g
Câu 28:
A. CnH2n+2 (n ≥ 1).
B. CnH2n (n ≥ 2).
C. CnH2n-2 (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
Đáp án: C
Giải thích:
Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là CnH2n-2
(n ≥ 2).
Câu 29:
A. 3
B. 5
C. 2
D. 4
Đáp án: A
Giải thích:
Độ bất bão hòa k = = 2
+ TH1: 1 liên kết ba
CH3 – CH(CH3) – C ≡ CH
+ TH2: 2 liên kết đôi
CH2 = C(CH3) – CH = CH3
CH3 – C(CH3) = C = CH2
→ Có 3 chất thỏa mãn đề bài.
Câu 30:
A. 35,8
B. 45,6
C. 38,2
D. 40,2
Đáp án: D
Giải thích:
Đốt cháy Y cũng là cháy X
BTNT “C”
→
Lại có:
→ tạo 2 muối Na2CO3 và NaHCO3
Trong đó
= 0,3 mol
→
m chất tan trong Z = 0,3.106 + 0,1.84 = 40,2g
Các câu hỏi trắc nghiệm Hóa học lớp 11 có đáp án, chọn lọc khác:
Trắc nghiệm Benzen và đồng đẳng. Một số hidrocacbon thơm khác có đáp án
Trắc nghiệm Luyện tập: Hiđrocacbon thơm có đáp án
Trắc nghiệm Nguồn hiđrocacbon thiên nhiên có đáp án
Trắc nghiệm Hệ thống hóa về hidrocacbon thiên nhiên có đáp án