Anonymous
0
0
Sách bài tập Hóa 11 Bài 17 (Chân trời sáng tạo): Phenol
- asked 6 months agoVotes
0Answers
0Views
Giải SBT Hóa 11 Bài 17: Phenol
Bài 17.1 trang 82 Sách bài tập Hóa học 11
Lời giải:
Đáp án đúng là: A
Công thức cấu tạo của phenol là C6H5OH.
Bài 17.2 trang 82 Sách bài tập Hóa học 11
B. meta, para.
C. ortho, meta, para.
D. ortho, para.
Lời giải:
Đáp án đúng là: D
Nhóm OH là nhóm đẩy e vào vòng benzene, làm giàu mật độ electron ở hai vị trí ortho và para.
Bài 17.3 trang 82 Sách bài tập Hóa học 11
A. ethanol.B. benzene.C. phenol.D. toluene.
Lời giải:
Đáp án đúng là: C
Ở điều kiện thường, chất tồn tại ở thể rắn là phenol.
Bài 17.4 trang 82 Sách bài tập Hóa học 11
A. Phenol là chất rắn, không màu hoặc màu hồng nhạt.
B. Phenol gây bỏng khi tiếp xúc với da, gây ngộ độc qua đường miệng.
C. Phenol không tan trong nước, nhưng tan trong ethanol.
D. Phenol có tính acid mạnh hơn ethanol.
Lời giải:
Đáp án đúng là: C
Phenol ít tan trong nước lạnh, tan vô hạn ở 66oC và tan tốt trong các dung môi hữu cơ.
Bài 17.5 trang 83 Sách bài tập Hóa học 11
B. dung dịch K2CO3.
C. kim loại Na.
D. kim loại Ag.
Lời giải:
Đáp án đúng là: C
2C6H5OH + 2Na → 2C6H5ONa + H2
Bài 17.6 trang 83 Sách bài tập Hóa học 11
B. Nước bromine.
C. Quỳ tím.
D. Phenolphthalein
Lời giải:
Đáp án đúng là: B
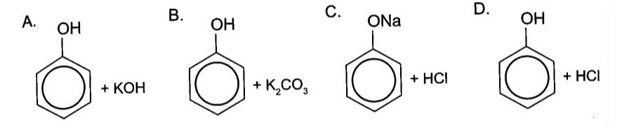
Bài 17.7 trang 83 Sách bài tập Hóa học 11
Lời giải:
Đáp án đúng là: D
Phenol có tính acid yếu nên không phản ứng với dung dịch HCl.
Bài 17.8 trang 83 Sách bài tập Hóa học 11
B. quỳ tím.
C. kim loại Na.
D. dung dịch NaOH.
Lời giải:
Đáp án đúng là: A
Phenol tạo kết tủa 2,4,6-tribromphenol khi phản ứng với dung dịch brom còn ethanol không phản ứng.
Bài 17.9 trang 83 Sách bài tập Hóa học 11
A. ethanol (C2H5OH).
B. phenol (C6H5OH).
C. benzene (C6H6).
D. toluene (C6H5CH3)
Lời giải:
Đáp án đúng là: B
PF là sản phẩm của phản ứng trùng ngưng giữa formaldehyde (H-CHO) với phenol (C6H5OH).
A. có hoạt tính sinh học.
B. chi phí thấp.
C. dễ bảo quản.
D. không gây độc nếu dùng dư liều lượng.
Lời giải:
Đáp án đúng là: A
Vì các hợp chất này có hoạt tính sinh học nên được sử dụng trong thuốc giảm ho, chất trị nám, chế biến thực phẩm, mĩ phẩm, dược phẩm.
Bài 17.11 trang 84 Sách bài tập Hóa học 11
STT |
Phát biểu |
Đúng/sai |
|
1 |
Phenol có nhóm chức -OH liên kết trực tiếp với nguyên tử carbon no. |
? |
|
2 |
Phenol đơn giản nhất có chứa một nguyên tử oxygen. |
? |
|
3 |
|
? |
|
4 |
Phenol (M = 94) và toluene (M = 92) có nhiệt độ nóng chảy tương đương nhau do khối lượng phân tử gần bằng nhau. |
? |
|
5 |
Phenol tạo được liên kết hydrogen với nước. |
? |
|
6 |
Phenol có tính acid, làm quỳ tím hoá màu đỏ. |
? |
|
7 |
Phenol tham gia phản ứng cộng với Br2 tạo thành 2,4,6-tribromophenol. |
? |
Lời giải:
STT |
Phát biểu |
Đúng/sai |
|
1 |
Phenol có nhóm chức -OH liên kết trực tiếp với nguyên tử carbon no. |
Sai |
|
2 |
Phenol đơn giản nhất có chứa một nguyên tử oxygen. |
Đúng |
|
3 |
|
Đúng |
|
4 |
Phenol (M = 94) và toluene (M = 92) có nhiệt độ nóng chảy tương đương nhau do khối lượng phân tử gần bằng nhau. |
Sai |
|
5 |
Phenol tạo được liên kết hydrogen với nước. |
Đúng |
|
6 |
Phenol có tính acid, làm quỳ tím hoá màu đỏ. |
Sai |
|
7 |
Phenol tham gia phản ứng cộng với Br2 tạo thành 2,4,6-tribromophenol. |
Sai |
Bài 17.12 trang 84 Sách bài tập Hóa học 11
Lời giải:
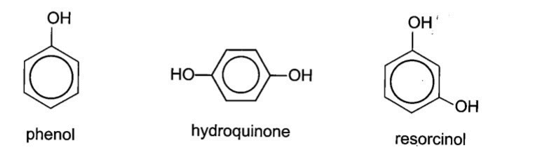
Trong nhiều trường hợp, có thể dựa vào khối lượng phân tử và số nhóm chức -OH trong hợp chốt phenol để so sánh nhiệt độ nóng chảy của các hợp chất. So với phenol, hydroquinone và resorcinol có khối lượng phân tử lớn hơn, tương tác van der Waals mạnh hơn; số nhóm chức -OH nhiều hơn, hình thành nhiều liên kết hydrogen hơn nên nhiệt độ nóng chảy của hydroquinone và resorcinol cao hơn phenol.
Đối với hydroquinone và resorcinol, nhiệt độ nóng chảy của các hợp chất còn phụ thuộc vào vị trí nhóm thế trên vòng benzene, hợp chất có tính đối xứng hơn sẽ có nhiệt độ nóng chảy cao hơn. Resorcinol (3-hydroxyphenol) và hydroquinone (4-hydroxyphenol) và đều có cùng khối lượng phân tử và số nhóm -OH, nhưng hydroquinone có nhiệt độ nóng chảy 172°C (do tính đối xứng trong phân tử), trong khi resorcinol là 110°C.
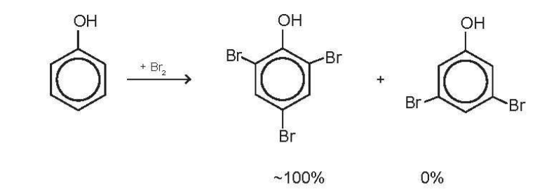
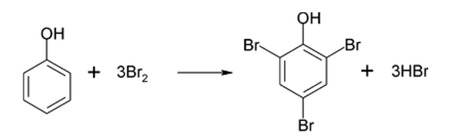
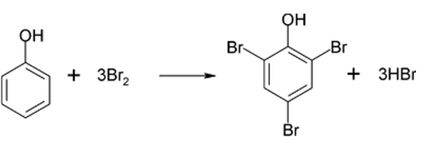
Bài 17.13 trang 84 Sách bài tập Hóa học 11: Trong thí nghiệm của phenol với nước Br2, thu được sản phẩm hữu cơ 2,4,6-tribromophenol (kết tủa màu trắng) đạt gần 100% và không thu được các sản phẩm thế bromo khác ở các vị trí còn lại của phenol. Giải thích. Cho sơ đồ minh hoạ như sau:
Lời giải:
Cặp electron của nguyên tử oxygen liên hợp với hệ thống electron vòng benzene, làm tăng mật độ electron vòng benzene, nhiều nhất ở các vị trí 2, 4, 6. Khi tham gia phản ứng thế với nước Br2, phenol ưu tiên thế các nguyên tử hydrogen ở vị trí 2, 4, 6.
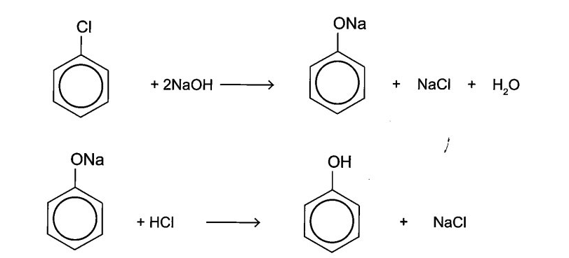
Bài 17.14 trang 85 Sách bài tập Hóa học 11: Trong công nghiệp, ngoài phương pháp điều chế phenol từ cumene hoặc từ nhựa than đá, người ta còn thực hiện điều chế bằng phản ứng, thuỷ phân dẫn xuất chlorobenzene với dung dịch NaOH đặc, ở nhiệt độ 350 °C, áp suất cao (quy trình Dow), sản phẩm hữu cơ là muối sodium phenolate, acid hoá bằng dung dịch HCl, thu được phenol.
a) Viết phương trình hoá học của các phản ứng xảy ra.
b) Tại sao khi thuỷ phân chlorobenzene không tạo thành sản phẩm trực tiếp phenol, mà tạo thành sodium phenolate?
Lời giải:
a) Phương trình hoá học của các phản ứng xảy ra:
b) Chlorobenzene tác dụng với NaOH, xảy ra phản ứng thế Cl bằng nhóm -OH tạo thành phenol, là một acid, phenol tác dụng với NaOH tạo thành muối sodium phenolate ngay sau đó.
Bài 17.15 trang 85 Sách bài tập Hóa học 11: Hằng số phân li acid Ka của một số hợp chất được thể hiện trong bảng dưới đây:
Hợp chất |
Ka(phân li trong H2O, 25oC) |
|
Phenol |
1,0 × 10-10 |
|
2-methylphenol |
6,3 × 10-11 |
|
2-chlorophenol |
7,8 × 10-9 |
|
2-nitrophenol |
6,8 × 10-8 |
|
2,4-dinitrophenol |
1,1 × 10-4 |
|
2,4,6- trinitrophenol (piric acid) |
0,4 |
|
Carbonic acid
|
5,0 × 10-7 5,0 × 10-11 |
a) Sắp xếp theo thứ tự giảm dần tính acid của các hợp chất phenol.
b) Trong các chất trên, chất nào tác dụng được với Na2CO3 sinh ra khí CO2? Giải thích.
Lời giải:
Hằng số phân li acid (Ka) càng lớn, tính acid càng mạnh.
a) Thứ tự giảm dần tính acid của các hợp chất: 2,4,6-trinitrophenol >
2,4-dinitrophenol > 2-nitrophenol > 2-chlorophenol > phenol > 2-methylphenol.
b) Hằng số phân li acid của quá trình :
Chất phản ứng với Na2CO3 sinh ra khí CO2 phải có tính acid mạnh hơn proton thứ nhất của H2CO3 hoặc có Ka lớn hơn 5×10-7.
Vậy chất phản ứng với Na2CO3 sinh ra khí CO2 là 2,4,6-trinitrophenol và 2,4-dinitrophenol.
Lời giải:
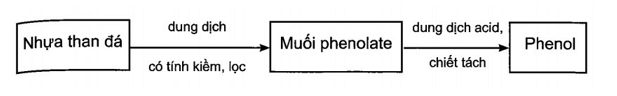
Dựa vào tính acid của phenol:
Nhựa than đá được trộn với dung dịch có tính kiềm (dung dịch kiềm, dung dịch amine,…), phenol phản ứng tạo thành phenolate, tan trong dung dịch và tách lớp với các thành phần còn lại. Dùng phương pháp chiết hoặc lọc để lấy tách dung dịch phenolate, acid hóa bằng dung dịch acid (H+), thu được phenol.
Dựa vào tính phân cực của phenol:
Phenol tan trong một số dung môi (hỗn hợp dung môi) phù hợp, tách lớp với thành phần còn lại, thu lấy dịch chiết, kết tinh, dùng máy li tâm để tách phenol (các chất phenol, cresol, xylenol, catechol, resorcinol gọi chung là phenol).
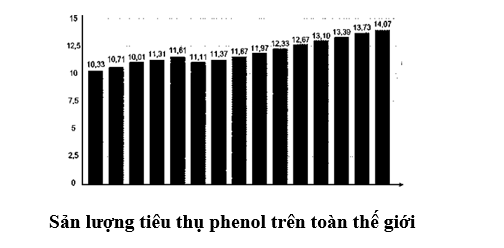
Để cung cấp đủ sản lượng tiêu thụ của phenol trong năm 2021, khối lượng cumene đã dùng để sản xuất phenol là bao nhiêu? (Chỉ tính trên lượng phenol đã tiêu thụ, không bao gồm lượng cumene thực tế sản xuất phenol chưa tiêu thụ).
Lời giải:
Sản lượng phenol sản xuất từ cumene là:
m = 90% × 11,37 = 10,233 (triệu tấn)
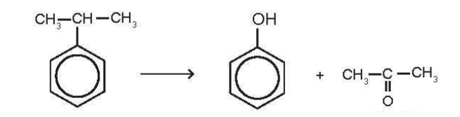
Sơ đồ điều chế phenol từ cumene:
Theo lí thuyết số mol cumene = số mol phenol :
Khối lượng cumene cần dùng là: (triệu tấn).
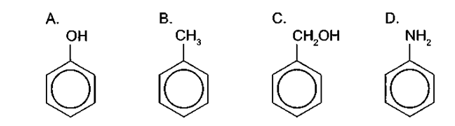
 không phải là alcohol.
không phải là alcohol.