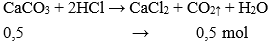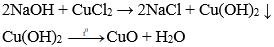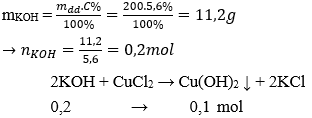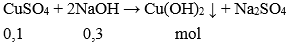Anonymous
0
0
TOP 40 câu Trắc nghiệm Tính chất hóa học của muối (có đáp án 2024) – Hóa học 9
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa học 9 Bài 9: Tính chất hóa học của muối
Bài giảng Hóa học 9 Bài 9: Tính chất hóa học của muối
Câu 1:
A. H2
B. CO2
C. SO2
D. NO2
Đáp án: C
Giải thích:
Phương trình phản ứng:
H2SO4 + Na2SO3 → Na2SO4 + SO2 ↑ + H2O
Vậy khí thu được là: SO2
Câu 2:
A. 26,7 gam
B. 27,6 gam
C. 28,8 gam
D. 29,4 gam
Đáp án: D
Giải thích:
Số mol của KOH là:
nKOH = 0,3.2 = 0,6 mol
Phương trình phản ứng:
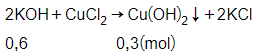
Theo phương trình phản ứng ta có:
= 0,3 mol
Khối lượng của Cu(OH)2 là:
= 0,3.98 = 29,4 gam.
Câu 3:
A. Tác dụng với kim loại
B. Tác dụng với axit
C. Tác dụng với dung dịch bazơ
D. A, B, C đều đúng
Đáp án: D
Giải thích:
Tính chất hóa học của muối là
+ Tác dụng với kim loại
+ Tác dụng với axit
+ Tác dụng với dung dịch bazơ
+ Tác dụng với dung dịch muối
+ Phản ứng phân hủy muối
Câu 4:
A. 4,89 gam
B. 5,91 gam
C. 6,19 gam
D. 5,45 gam
Đáp án: B
Giải thích:
Khối lượng của Ba(OH)2 có trong dung dịch là:
Số mol của Ba(OH)2 là:
= 0,03 mol
Phương trình phản ứng:
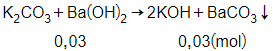
Theo phương trình phản ứng ta có:
= 0,03 mol
Khối lượng của BaCO3 là:
m = 0,03.197 = 5,91 gam.
Câu 5:
A. Có khí thoát ra
B. Xuất hiện kết tủa màu trắng
C. Xuất hiện kết tủa xanh lam
D. Xuất hiện kết tủa màu đỏ nâu
Đáp án: D
Giải thích:
Cho dung dịch NaOH vào ống nghiệm đựng dung dịch FeCl3, xảy ra phản ứng hóa học:
![]()
Quan sát hiện tượng thấy xuất hiện kết tủa màu đỏ nâu là: Fe(OH)3
Câu 6:
A. 7,84 lít
B. 6,72 lít
C. 5,56 lít
D. 4,90 lít
Đáp án: A
Giải thích:
Số mol của CaCO3 là:
= 0,35 mol
Phương trình phản ứng:
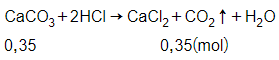
Theo phương trình phản ứng ta có:
= 0,35 mol
Thể tích khí CO2 ở đktc là:
= 0,35.22,4 = 7,84 lít.
Câu 7:
A. KClO3
B. KMnO4
C. CaCO3
D. A, B, C đều đúng
Đáp án: D
Giải thích:
Phương trình phản ứng:
2KClO3 2KCl +3O2
2KMnO4 MnO2 + O2 + K2MnO4
CaCO3 CaO + CO2
Câu 8:
(1) Muối tác dụng với axit tạo thành muối mới và axit mới.
(2) Hai dung dịch muối tác dụng với nhau tạo thành hai muối mới.
(3) Phản ứng trao đổi là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
(4) Phản ứng trung hòa không thuộc loại phản ứng trao đổi.
Số phát biểu đúng là
A. 1
B. 2
C. 3
D. 4
Đáp án: C
Giải thích:
Số phát biểu đúng là: (1), (2), (3)
Phát biểu (4) sai vì phản ứng trung hòa cũng thuộc loại phản ứng trao đổi và luôn xảy ra.
Câu 9:
A. 41,8 gam
B. 42,5 gam
C. 43,2 gam
D. 44.6 gam
Đáp án: C
Giải thích:
Số mol của Cu là:
nCu = 0,2 mol
Phương trình phản ứng:
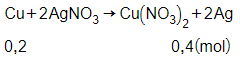
Theo phương trình phản ứng ta có:
nAg = 0,4.108 = 43,2 gam.
Câu 10:
BaCO3 + 2HCl → BaCl2 + Y + H2O
Vậy Y là
A. CO
B. H2
C. Cl2
D. CO2
Đáp án: D
Giải thích:
Phương trình phản ứng:
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
Câu 11:
A. 22,04 lít
B. 19,69 lít
C. 21,04 lít
D. 20,16 lít
Đáp án: D
Giải thích:
Số mol của KClO3 là:
= 0,6 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có:
= 0,9 mol
Vậy thể tích của O2 là:
V = 0,9.22,4 = 20,16 lít.
Câu 12:
A. Muối nitrat
B. Muối sunfat
C. Muối clorua
D. Muối cacbonat không tan
Đáp án: D
Giải thích:
Muối cacbonat không tan bị nhiệt phân hủy tạo ra hợp chất oxit và một chất khí làm đục nước vôi trong.
Ví dụ:
CaCO3 CaO + CO2
Khí CO2 sinh ra làm đục nước vôi trong:
CO2 + Ca(OH)2 →CaCO3 ↓ + H2O
Câu 13:
AgNO3 + NaCl → NaNO3 + AgCl↓
Tích các hệ số cân bằng (là các số nguyên, tối giản) trong phương trình phản ứng trên là
A. 1
B. 2
C. 3
D. 4
Đáp án: A
Giải thích:
Phương trình phản ứng:
AgNO3 + NaCl → NaNO3 + AgCl↓
Tích các hệ số cân bằng (là các số nguyên, tối giản) trong phương trình phản ứng trên là: 1.1.1.1 = 1
Câu 14:
A. 16,8 gam
B. 17,6 gam
C. 18,6 gam
D. 19,4 gam
Đáp án: A
Giải thích:
Phương trình phản ứng:
MgCO3 MgO + CO2
Áp dụng định luật bảo toàn khối lượng ta có:
= 16,8 gam
Vậy m = 16,8 gam
Câu 15:
A. BaCl2, CaCO3
B. NaCl, Cu(NO3)2
C. Cu(NO3)2, Na2CO3
D. NaCl, BaCl2
Đáp án: A
Giải thích:
Phương trình phản ứng:
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
CaCO3 + H2SO4 → CaSO4 + CO2↑ + H2O
Câu 16: Cho dung dịch axit sunfuric loãng tác dụng với muối natrisunfit (Na2SO3). Chất khí nào sinh ra ?
A. Khí hiđro
B. Khí oxi
C. Khí lưu huỳnh đioxit
D. Khí hiđro sunfua
Đáp án: C
Giải thích:
Na2SO3 + H2SO4 → Na2SO4 v+ SO2↑ + H2O
Câu 17: Cho 50 g CaCO3 vào dung dịch HCl dư thể tích CO2 thu được ở đktc là:
A. 11,2 lít
B. 1,12 lít
C. 2,24 lít
D. 22,4 lít
Đáp án: A
Giải thích:
Số mol CaCO3 = 50 : 100 = 0,5 mol
→ Vkhí = n.22,4 = 0,5.22,4 = 11,2 lít.
Câu 18: Cho dung dịch KOH vào ống nghiệm đựng dung dịch FeCl3, hiện tượng quan sát được là:
A. Có kết tủa trắng xanh.
B. Có khí thoát ra.
C. Có kết tủa đỏ nâu.
D. Kết tủa màu trắng.
Đáp án: C
Giải thích:
3KOH + FeCl3 → 3KCl + Fe(OH)3 (↓ đỏ nâu)
Câu 19: Hãy cho biết muối nào có thể điều chế bằng phản ứng của kim loại với dung dịch axit H2SO4 loãng ?
A. ZnSO4
B. Na2SO3
C. CuSO4
D. MgSO3
Đáp án: A
Giải thích:
Zn + H2SO4 (loãng) → ZnSO4 + H2
Câu 20:Cặp chất nào sau đâykhôngthể tồn tại trong 1 dung dịch (do có phản ứng với nhau) ?
A. NaOH, MgSO4
B. KCl, Na2SO4
C. CaCl2, NaNO3
D. ZnSO4, H2SO4
Đáp án: A
Giải thích:
2NaOH + MgSO4 → Mg(OH)2 ↓ + Na2SO4
Câu 21: Nếu chỉ dùng dung dịch NaOH thì có thể phân biệt được 2 dung dịch muối trong mỗi cặp chất sau:
A. Na2SO4 và Fe2(SO4)3
B. Na2SO4 và K2SO4
C. Na2SO4 và BaCl2
D. Na2CO3 và K3PO4
Đáp án: A
Giải thích:
Sử dụng NaOH có thể phân biệt được cặp Na2SO4 và Fe2(SO4)3
+ Nếu không có hiện tượng gì → Na2SO4
+ Nếu xuất hiện kết tủa đỏ nâu → Fe2(SO4)3
6NaOH + Fe2(SO4)3 → 2Fe(OH)3 (↓ đỏ nâu) + 3Na2SO4.
Câu 22: Nhỏ từ từ dung dịch NaOH vào dung dịch CuCl2 đển khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn nào sau đây:
A. Cu
B. CuO
C. Cu2O
D. Cu(OH)2.
Đáp án: B
Giải thích:
Câu 23: Cho 200g dung dịch KOH 5,6% vào dung dịch CuCl2 dư, sau phản ứng thu được lượng chất kết tủa là:
A. 19,6 g
B. 9,8 g
C. 4,9 g
D. 17,4 g
Đáp án: B
Giải thích:
→ Khối lượng kết tủa: m↓ = 0,1. (64 + 17.2) = 9,8 gam.
Câu 24: Trộn dung dịch có chứa 0,1mol CuSO4 và một dung dịch chứa 0,3 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m g chất rắn. Giá trị m là:
A. 8 g
B. 4 g
C. 6 g
D. 12 g
Đáp án: A
Giải thích:
Theo PTHH có NaOH dư → số mol Cu(OH)2 tính theo số mol CuSO4
→ m = 0,1.80 = 8 gam.
Câu 25: Trộn 2 dung dịch nào sau đây sẽ không xuất hiện kết tủa ?
A. BaCl2, Na2SO4
B. Na2CO3, Ba(OH)2
C. BaCl2, AgNO3
D. NaCl, K2SO4
Đáp án: D
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Một số muối quan trọng có đáp án
Trắc nghiệm Phân bón hóa học có đáp án
Trắc nghiệm Mối liên hệ giữa các loại chất vô cơ có đáp án
Trắc nghiệm Luyện tập chương 1: Các hợp chất vô cơ có đáp án