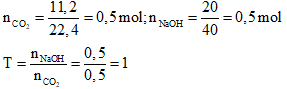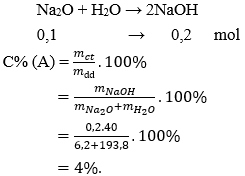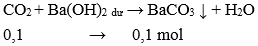Anonymous
0
0
TOP 40 câu Trắc nghiệm Mối liên hệ giữa các loại chất vô cơ (có đáp án 2024) - Hóa học 9
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa học 9 Bài 12: Mối quan hệ giữa các loại chất vô cơ
Bài giảng Hóa học 9 Bài 12: Mối quan hệ giữa các loại chất vô cơ
Câu 1:
A. CuO
B. Na2O
C. BaO
D. SO2
Đáp án: D
Giải thích:
Phương trình phản ứng:
SO2 + H2O → H2SO3
Câu 2:
A. SO2
B. CO2
C. NO2
D. CaO
Đáp án: D
Giải thích:
Phương trình phản ứng:
CaO + H2O→ Ca(OH)2
Câu 3:
A. 19,9 gam
B. 20, 8 gam
C. 21, 6 gam
D. 22,4 gam
Đáp án: D
Giải thích:
Số mol của K2O là:
= 0,2 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có:
nKOH = 0,4 mol
Vậy khối lượng KOH là:
m = 0,4.56 = 22,4 gam.
Câu 4:
A. Cho Na2SO4 tác dụng với Ba(OH)2
B. Cho Na2O tác dụng với HCl
C. Cho kim loại Na tác dụng với nước
D. Cho Na2O tác dụng với H2O
Đáp án: B
Giải thích:
NaOH không được tạo thành trong thí nghiệm: cho Na2O tác dụng với HCl
Vì Na2O + 2HCl → 2NaCl + H2O
Câu 5:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án: C
Giải thích:
Số mol của Na2SO3 là:
= 0,15 mol
Phương trình phản ứng:
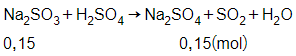
Theo phương trình phản ứng ta có:
= 0,15 mol
Vậy thể tích của SO2 là:
= 0,15.22,4 = 3,36 lít.
Câu 6:
A. Na2CO3.
B. NaHCO3.
C. Hỗn hợp Na2CO3 và NaHCO3.
D. Na(HCO3)2.
Đáp án: B
Giải thích:
→ Sau phản ứng thu được muối NaHCO3.
Câu 7:
A. CO
B. NO2
C. Na2O
D. P2O5
Đáp án: C
Giải thích:
pH > 7: Dung dịch có tính bazơ
Phương trình phản ứng:
Na2O + H2O → 2NaOH
Câu 8:
Thể tích dung dịch HCl đã dùng là
A. 0,2 lít
B. 0,3 lít
C. 0,4 lít
D. 0,5 lít
Đáp án: A
Giải thích:
Số mol của MgCO3 là:
= 0,3 mol
Phương trình phản ứng:
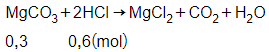
Theo phương trình phản ứng ta có:
nHCl = 0,6 mol
Thể tích dung dịch HCl đã dùng là:
VHCl = = 0,2 lít
Câu 9:
A. Dung dịch AgNO3
B. Dung dịch HCl
C. Dung dịch BaCl2
D. Dung dịch NaOH
Đáp án: D
Giải thích:
Dung dịch tác dụng được với Fe(NO3)2 và CuCl2 là dung dịch NaOH.
Phương trình phản ứng:
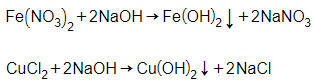
Câu 10:
A. 9,85 gam
B. 10,05 gam
C. 11.20 gam
D. 8,45 gam
Đáp án: A
Giải thích:
Số mol của CO2 là:
= 0,05 mol
Phương trình phản ứng:
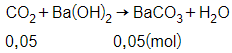
Số mol của BaCO3 là:
= 0,05 mol
Vậy khối lượng của BaCO3 là:
= 0,05.197 = 9,85 gam.
Câu 11:
A. CaO
B. K2O
C. CuO
D. SO2
Đáp án: D
Giải thích:
pH <7: dung dịch có tính axit
Phương trình phản ứng:
SO2 + H2O → H2SO3
Câu 12:
A. 20,6 gam
B. 21,4 gam
C. 22,2 gam
D. 23,6 gam
Đáp án: B
Giải thích:
Số mol KOH là:
nKOH = 0,6 mol
Phương trình phản ứng:
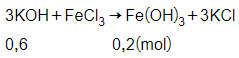
Số mol Fe(OH)3 là:
= 0,2 mol
Vậy khối lượng Fe(OH)3 là
m = 0,2.107 = 21,4 gam.
Câu 13:
A. Dung dịch K2SO4 và dung dịch BaCl2
B. Dung dịch K2SO4 và dung dịch KCl
C. Dung dịch K2SO4 và dung dịch Fe2(SO4)3
D. Dung dịch K2SO4 và dung dịch K2CO3
Đáp án: C
Giải thích:
Khi cho KOH vào hai dung dịch:
+) Chỉ Fe2(SO4)3 xuất hiện kết tủa nâu đỏ
Phương trình phản ứng:
6KOH + Fe2(SO4)3 → 2Fe(OH)3 ↓ + 3K2SO4
+) K2SO4 không có hiện tượng.
Câu 14:
A. MgSO3
B. ZnSO4
C. Na2SO3
D. CuSO4
Đáp án: B
Giải thích:
Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Chú ý: Cu không phản ứng với H2SO4 loãng nên không điều chế CuSO4 bằng cách này.
Câu 15:
A. Ba(OH)2
B. HCl
C. NaCl
D. KOH
Đáp án: A
Giải thích:
Dung dịch chất Y có pH > 7 nên Y có môi trường bazơ.
Vậy Y có thể là Ba(OH)2 hoặc KOH.
Mà dung dịch Y tác dụng với dung dịch Na2SO4 tạo kết tủa nên chất Y là Ba(OH)2
Phương trình phản ứng:
Ba(OH)2 + Na2SO4 → BaSO4 ↓ + 2NaOH
Câu 16: Chất tác dụng với nước tạo ra dung dịch bazơ là:
A. K2O.
B. CuO.
C. CO.
D. SO2.
Đáp án: A
Giải thích:
K2O + H2O → 2KOH.
Câu 17: Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO,
B. BaO,
C. Na2O
D. SO3.
Đáp án: D
Giải thích:
SO3 + H2O → H2SO4.
Câu 18: Dãy oxit tác dụng với nước tạo ra dung dịch kiềm:
A. CuO, CaO, K2O, Na2O.
B. CaO, Na2O, K2O, BaO.
C. Na2O, BaO, CuO, MnO.
D. MgO, Fe2O3, ZnO, PbO.
Đáp án: B
Câu 19: Dãy oxit tác dụng với dung dịch NaOH:
A. CuO, Fe2O3, SO2, CO2.
B. CaO, CuO, CO, N2O5.
C. CO2, SO2, P2O5, SO3.
D. SO2, MgO, CuO, Ag2O.
Đáp án: C
Giải thích:
Oxit axit (CO2, SO2, P2O5, SO3) tác dụng được với dung dịch NaOH.
Câu 20: Dãy oxit vừa tác dụng với nước, vừa tác dụng với dung dịch axit là:
A. CuO, Fe2O3, SO2, CO2.
B. CaO, CuO, CO, N2O5.
C. CaO, Na2O, K2O, BaO.
D. SO2, MgO, CuO, Ag2O.
Đáp án: C
Câu 21: Hấp thụ hoàn toàn 11,2 lít khí CO2 (đktc) bằng một dung dịch chứa 20 g NaOH. Muối được tạo thành là:
A. Na2CO3.
B. NaHCO3.
C. Hỗn hợp Na2CO3 và NaHCO3.
D. Na(HCO3)2.
Đáp án: B
Giải thích:
→ Sau phản ứng thu được muối NaHCO3.
Câu 22: Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Nồng độ phần trăm của dung dịch A là:
A. 4%.
B. 6%.
C. 4,5%
D. 10%
Đáp án: A
Giải thích:
Số mol Na2O = 6,2 : 62 = 0,1 mol
Câu 23: Oxit nào sau đây khi tác dụng với nước tạo ra dung dịch có pH > 7 ?
A. CO2
B. SO2
C. CaO
D. P2O5
Đáp án: C
Giải thích:
CaO + H2O → Ca(OH)2
Dung dịch Ca(OH)2 có pH > 7.
Câu 24: Cho 2,24 lít CO2 (đktc) tác dụng với dung dịch Ba(OH)2 dư. Khối lượng chất kết tủa thu được là :
A. 19,7 g
B. 19,5 g
C. 19,3 g
D. 19 g
Đáp án: A
Giải thích:
Số mol CO2 = 2,24 : 22,4 = 0,1 mol
→ m↓ = 0,1.197 = 19,7 gam.
Câu 25: Dùng thuốc thử nào sau đây để phân biệt các chất chứa trong các ống nghiệm mất nhãn: HCl, KOH, NaNO3, Na2SO4.
A. Dùng quì tím và dung dịch CuSO4.
B. Dùng dung dịch phenolphtalein và dung dịch BaCl2.
C. Dùng quì tím và dung dịch BaCl2.
D. Dùng dung dịch phenolphtalein và dung dịch H2SO4.
Đáp án: C
Giải thích:
- Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl.
+ Quỳ tím chuyển sang màu xanh → KOH.
+ Quỳ tím không chuyển màu → NaNO3 và Na2SO4.
- Phân biệt NaNO3 và Na2SO4: Dùng BaCl2
+ Xuất hiện kết tủa trắng → Na2SO4.
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
+ Không hiện tượng → NaNO3.
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Luyện tập chương 1: Các hợp chất vô cơ có đáp án
Trắc nghiệm Tính chất vật lí của kim loại có đáp án
Trắc nghiệm Tính chất hóa học của kim loại có đáp án