Anonymous
0
0
Khoa học tự nhiên 7 Bài 6 (Cánh diều): Hóa trị, công thức hóa học
- asked 6 months agoVotes
0Answers
0Views
Giải bài tập Khoa học tự nhiên 7 Bài 6: Hóa trị, công thức hóa học
Bài giảng Khoa học tự nhiên 7 Bài 6: Hóa trị, công thức hóa học
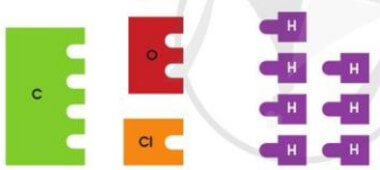
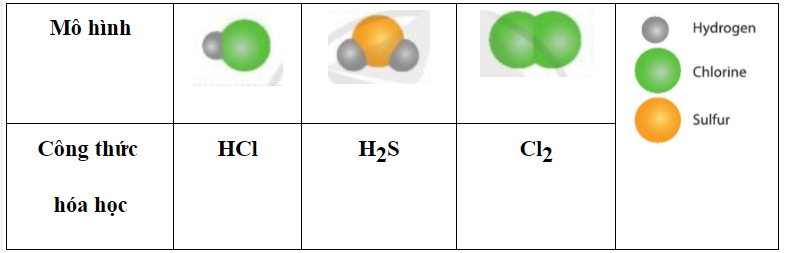
Mở đầu trang 39 Bài 6 KHTN lớp 7: Cho các miếng bìa ghi kí hiệu hóa học của các nguyên tố C, O, Cl, H như hình dưới đây. Mỗi miếng bìa tượng trưng cho một nguyên tử. Hãy ghép các miếng bìa H với các miếng bìa khác sao cho phù hợp.
Trả lời:
I. Hóa trị
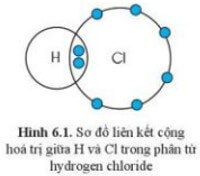
Câu hỏi 1 trang 39 KHTN lớp 7: Quan sát hình 6.1, hãy so sánh hóa trị của nguyên tố và số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết.
Trả lời:
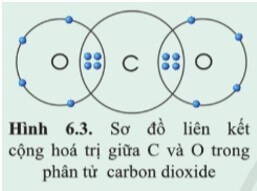
Luyện tập 1 trang 40 KHTN lớp 7: Quan sát hình 6.3 và xác định hóa trị của C và O trong khí carbon dioxide
Trả lời:
- Nguyên tử C góp chung 4 electron để hình thành liên kết ⇒ C có hóa trị IV.
Luyện tập 2 trang 40 KHTN lớp 7: Vẽ sơ đồ hình thành liên kết giữa nguyên tử N và ba nguyên tử H. Hãy cho biết liên kết đó thuộc loại liên kết nào. Hóa trị của mỗi nguyên tố trong hợp chất được tạo thành là bao nhiêu?
Trả lời:
Câu hỏi 2 trang 41 KHTN lớp 7: Cát được sử dụng nhiều trong xây dựng và là nguyên liệu chính để sản xuất thủy tinh. Silicon oxide là thành phần chính của cát. Phân tử silicon oxide gồm 1 nguyên tử Si liên kết với 2 nguyên tử O. Dựa vào hóa trị của các nguyên tố trong bảng 6.1, hãy tính tích hóa trị và số nguyên tử của mỗi nguyên tố trong phân tử silicon oxide. Nhận xét về tích đó.
Trả lời:
|
Nguyên tố |
Si |
O |
|
Hóa trị |
IV |
II |
|
Số nguyên tử |
1 |
2 |
|
Tích hóa trị và số nguyên tử |
IV × 1 = II × 2 | |
Tích của hóa trị và số nguyên tử tham gia liên kết của Si và O bằng nhau.
Luyện tập 3 trang 41 KHTN lớp 7: Dựa vào hóa trị của các nguyên tố trong bảng 6.1 và quy tắc hóa trị, hãy cho biết mỗi nguyên tử Mg có thể kết hợp được với bao nhiêu nguyên tử Cl.
Trả lời:
|
Nguyên tố |
Mg |
Cl |
|
Hóa trị |
II |
I |
|
Số nguyên tử |
1 |
y |
|
Tích hóa trị và số nguyên tử |
II × 1 = I × y | |
Ta có: II × 1 = I × y ⇒ y = 2
Vậy mỗi nguyên tử Mg có thể kết hợp được với 2 nguyên tử Cl.
Luyện tập 4 trang 41 KHTN lớp 7: Nguyên tố A có hóa trị III, nguyên tố B có hóa trị II. Hãy tính tỉ lệ nguyên tử của A và B trong hợp chất tạo thành từ hai nguyên tố đó.
Trả lời:
|
Nguyên tố |
A |
B |
|
Hóa trị |
III |
II |
|
Số nguyên tử |
x |
y |
|
Tích hóa trị và số nguyên tử |
III × x = II × y | |
Ta có: III × x = II × y ⟺
Vậy tỉ lệ nguyên tử của A và B trong hợp chất tạo thành từ hai nguyên tố đó là 2 : 3
II. Công thức hóa học
Câu hỏi 3 trang 41 KHTN lớp 7: Cho công thức hóa học của một số chất như sau:
Xác định nguyên tố tạo thành mỗi chất và số nguyên tử của mỗi nguyên tố có trong phân tử.
Trả lời:
Luyện tập 5 trang 42 KHTN lớp 7: Viết công thức hóa học của các chất:
a) Sodium sulfide, biết trong phân tử có hai nguyên tử Na và một nguyên tử S.
b) Phosphoric acid, biết trong phân tử có ba nguyên tử H, một nguyên tử P và bốn nguyên tử O.
Trả lời:
a) Sodium sulfide: Na2S
b) Phosphoric acid: H3PO4
Luyện tập 6 trang 42 KHTN lớp 7: Viết công thức hóa học cho các chất được biểu diễn bằng những mô hình sau. Biết mỗi quả cầu biểu diễn cho một nguyên tử
|
Mô hình |
|
|
|
|
|
Công thức hóa học |
? |
? |
? |
Trả lời:
Luyện tập 7 trang 42 KHTN lớp 7: Đường glucose là nguồn cung cấp năng lượng quan trọng cho hoạt động sống của con người. Đường glucose có công thức hóa học là C6H12O6. Hãy cho biết:
a) Glucose được tạo thành từ những nguyên tố nào?
b) Khối lượng mỗi nguyên tố trong một phân tử glucose bằng bao nhiêu?
c) Khối lượng phân tử glucose là bao nhiêu?
Trả lời:
Câu hỏi 4 trang 43 KHTN lớp 7: Có ý kiến cho rằng: Trong nước, số nguyên tử H gấp hai lần số nguyên tử O nên phần trăm khối lượng của H trong nước gấp hai lần phần trăm khối lượng của O. Theo em, ý kiến trên có đúng không? Hãy tính phần trăm khối lượng của H, O trong nước để chứng minh.
Trả lời:
%mH =
Phần trăm về khối lượng của O trong H2O là:
%mO = = = 88,89%
Vậy ý kiến cho rằng: “Trong nước, số nguyên tử H gấp hai lần số nguyên tử O nên phần trăm khối lượng của H trong nước gấp hai lần phần trăm khối lượng của O” là không đúng.
Luyện tập 8 trang 43 KHTN lớp 7: Calcium carbonate là thành phần chính của đá vôi, có công thức hóa học là CaCO3. Tính phần trăm khối lượng của mỗi nguyên tố trong hợp chất trên.
Trả lời:
Khối lượng của nguyên tố Ca trong CaCO3 là:
mCa = 1 × 40 amu = 40 amu
Khối lượng của nguyên tố C trong CaCO3 là:
mC = 1 × 12 amu = 12 amu
Khối lượng của nguyên tố O trong CaCO3 là:
mO = 3 × 16 = 48 amu
→ Khối lượng phân tử CaCO3 là: = 40 + 12 + 48 = 100 amu
Phần trăm về khối lượng của Ca trong CaCO3 là:
%mCa =
Phần trăm về khối lượng của C trong CaCO3 là:
%mC = = = 12%
Phần trăm về khối lượng của O trong CaCO3 là:
%mO =
Luyện tập 9 trang 43 KHTN lớp 7: Citric acid là hợp chất được sử dụng nhiều trong công nghiệp thực phẩm, dược phẩm. Trong tự nhiên, citric acid có trong quả chanh và một số loại quả như bưởi, cam, … Citric acid có công thức hóa học là C6H8O7. Hãy tính phần trăm khối lượng của mỗi nguyên tố trong citric acid.
Trả lời:
Phần trăm về khối lượng của C trong C6H8O7 là:
%mC =
Phần trăm về khối lượng của H trong C6H8O7 là:
%mH = × 100% = × 100% = 4,17%
Phần trăm về khối lượng của O trong C6H8O7 là:
%mO =
Vận dụng trang 43 KHTN lớp 7: Potassium (kali) rất cần thiết cho cây trồng, đặc biệt trong giai đoạn cây trưởng thành, ra hoa, kết trái. Để cung cấp K cho cây có thể sử dụng phân potassium chloride và potassium sulfate có công thức hóa học lần lượt là KCl và K2SO4. Người trồng cây muốn sử dụng loại phân bón có hàm lượng K cao hơn thì nên chọn loại phân bón nào?
Trả lời:
- Xét hợp chất KCl ta có:
Khối lượng K trong hợp chất KCl là:
mK = 1 × 39 amu = 39 amu
Khối lượng phân tử hợp chất KCl là:
MKCl = 1 × 39 + 1 × 35,5 = 74,5 amu
Phần trăm khối lượng của K trong hợp chất KCl là:
%mK = = = 52,35%
- Xét hợp chất K2SO4 ta có:
Khối lượng K trong hợp chất K2SO4 là
mK = 2 × 39 amu = 78 amu
Khối lượng phân tử hợp chất K2SO4 là
= 2 × 39 amu + 1 × 32 amu + 4 × 16 amu = 174 amu
Phần trăm khối lượng của K trong hợp chất K2SO4 là
%mK = = = 44,83%
Vậy người trồng cây muốn sử dụng loại phân bón có hàm lượng K cao hơn nên dùng phân KCl.
Luyện tập 10 trang 44 KHTN lớp 7: Xác định hóa trị của mỗi nguyên tố trong các hợp chất sau: HBr, BaO
Trả lời:
Luyện tập 11 trang 45 KHTN lớp 7: Hợp chất X được tạo thành bởi Fe và O có khối lượng phân tử là 160 amu. Biết phần trăm khối lượng của Fe trong X là 70%. Hãy xác định công thức hóa học của X.
Trả lời:
Đặt công thức hóa học của X là FexOy
Khối lượng nguyên tố Fe trong một phân tử X là
(amu)
Khối lượng của nguyên tố S trong một phân tử X là
160 – 112 = 48 (amu)
Ta có: 56 amu × x = 112 amu → x = 2
16 amu × y = 48 amu → y = 3
Vậy công thức hóa học của X là Fe2O3
Lý thuyết Khoa học tự nhiên 7 Bài 6: Hóa trị, công thức hóa học
I. Hóa trị
1. Khái niệm về hóa trị
- Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác.
Ví dụ:
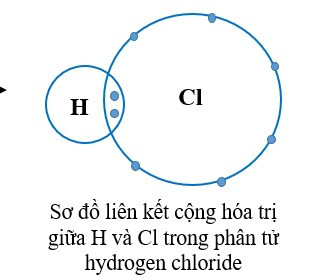
+ Trong phân tử hydrogen chloride, mỗi nguyên tử H và Cl góp chung 1 electron tạo ra đôi electron dùng chung giữa hai nguyên tử nên H và Cl có hóa trị I.
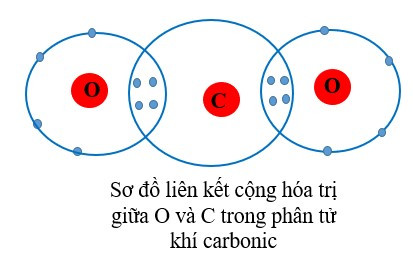
+ Trong phân tử khí carbonic, mỗi nguyên tử O góp chung 2 electron, nguyên tử C góp chung 4 electron. Như vậy nguyên tử C liên kết với 2 nguyên tử O bằng 4 đôi electron chung nên C có hóa trị IV và O có hóa trị II.
- Thông thường, hóa trị của nguyên tố trong hợp chất cộng hóa trị = số electron mà nguyên tử nguyên tố đó góp chung với nguyên tố khác.
- Trong hợp chất, H luôn có hóa trị I, O luôn có hóa trị II.
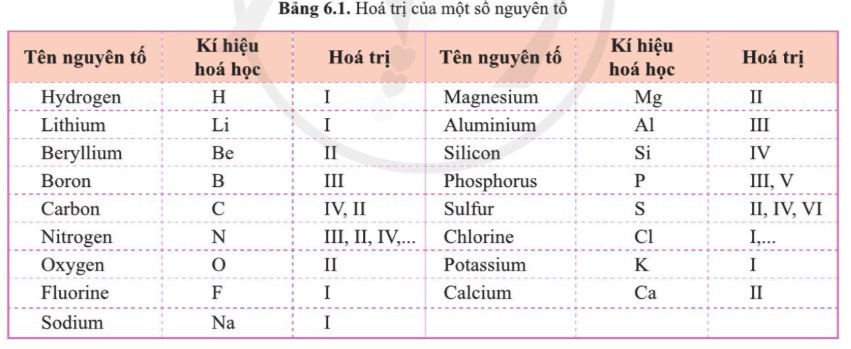
- Hóa trị của một số nguyên tố:
- Hóa trị của một số nhóm nguyên tử

2. Quy tắc hóa trị
- Quy tắc hóa trị: Khi các nguyên tử của hai nguyên tố A, B liên kết với nhau, tích giữa hóa trị và số nguyên tử của A bằng tích giữa hóa trị và số nguyên tử của B.
Ví dụ:
+ Trong phân tử nước, hóa trị và số nguyên tử tham gia liên kết của H và O như sau:
|
Nguyên tố |
H |
O |
|
Hóa trị |
I |
II |
|
Số nguyên tử |
2 |
1 |
|
Tích hóa trị và số nguyên tử |
I × 2 = II × 1 | |
+ Trong phân tử sulfur dioxide (SO2), hóa trị và số nguyên tử tham gia liên kết của S và O như sau:
|
Nguyên tố |
S |
O |
|
Hóa trị |
IV |
II |
|
Số nguyên tử |
1 |
2 |
|
Tích hóa trị và số nguyên tử |
IV × 1 = II × 2 | |
II. Công thức hóa học
1. Công thức hóa học
- Công thức hóa học dùng để biểu diễn chất.
- Công thức hóa học gồm hai phần:
+ Phần chữ: gồm kí hiệu hóa học của nguyên tố tạo thành chất.
+ Phần số: gồm các số được ghi bên phải, dưới chân kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong một phân tử (nếu chỉ có một nguyên tử thì không ghi). Các số này được gọi là chỉ số.

- Công thức hóa học của hợp chất có hai kí hiệu hóa học trở lên.
Ví dụ: NaCl, CaO, HNO3, BaSO4,…
- Công thức hóa học của các đơn chất chỉ có một kí hiẹu hóa học.
+ Với phi kim, phân tử thường có hai nguyên tử.
Ví dụ: N2, H2, O2, Br2,…
+ Với kim loại và một số phi kim, kí hiệu hóa học của nguyên tố được coi là công thức hóa học của đơn chất.
Ví dụ: Kim loại: Fe, Cu, Al, Mg,… và phi kim: C, S, P,…
2. Ý nghĩa của công thức hóa học
Công thức hóa học của một số chất cho biết một số thông tin
+ Nguyên tố tạo ra chất.
+ Số nguyên tử của mỗi nguyên tố có trong một phân tử chất.
+ Khối lượng phân tử của chất.
Ví dụ: Công thức hóa học của nitric acid là HNO3:
+ Nitric acid được tạo thành từ H, N và O.
+ Trong một phân tử nitric acid có 1 nguyên tử H, 1 nguyên tử N và 3 nguyên tử O.
+ Khối lượng phân tử của nitric là:
1 × 1 amu + 1 × 14 amu + 3 × 16 amu = 63 amu
Biết công thức hóa học tính được phần trăm khối lượng các nguyên tố trong hợp chất
- Khi biết công thức hóa học của một chất, tính được thành phần phần trăm khối lượng của các nguyên tố tạo ra chất theo các bước sau:
+ Tính khối lượng mỗi nguyên tố có trong một phân tử hợp chất.
+ Tính khối lượng phân tử.
+ Tính phần trăm khối lượng của nguyên tố theo công thức:
(Khối lượng nguyên tố : Khối lượng phân tử hợp chất) × 100%
Ví dụ: Tính phần trăm khối lượng của Cu, O trong hợp chất CuO.
Hướng dẫn giải:
Ta có: Khối lượng của nguyên tố O trong CuO là:
mO = 1 × 16 amu = 16 amu
Khối lượng của nguyên tố Cu trong CuO là:
mCu = 1 × 64 amu = 64 amu
Khối lượng của phân tử CuO là: MCuO = 16 + 64 = 80 (amu)
Phần trăm khối lượng của Cu trong hợp chất CuO là:
Phần trăm về khối lượng của O trong hợp chất CuO là:
%mO = 100% - %mCu = 100% - 80% = 20%
Biết công thức hóa học và hóa trị của một nguyên tố, xác định được hóa trị của nguyên tố còn lại trong hợp chất
- Cách xác định hóa trị khi biết công thức hóa học và hóa trị của một nguyên tố:
+ Đặt hóa trị của nguyên tố chưa biết là a.
+ Xác định a dựa vào quy tắc hóa trị.
Ví dụ: Xác định hóa trị của Al trong hợp chất có công thực hóa học Al2O3.
Giải:
Gọi hóa trị của Al trong hợp chất là a.
Vì O có hóa trị II nên ta có biểu thức: a × 2 = II × 3 → a = III
Vậy Al có hóa trị III trong hợp chất Al2O3.
3. Xác định công thức hóa học của hợp chất khi biết hóa trị hoặc phần trăm khối lượng của các nguyên tố
a) Biết hóa trị của các nguyên tố, lập công thức hóa học của hợp chất tạo thành từ hai nguyên tố
- Nếu hai nguyên tố A, B có hóa trị tương ứng là a, b thì công thức hóa học của hợp chất tạo thành từ A và B được xác định như sau:
+ Đặt công thức hóa học của hợp chất AxBy.
+ Áp dụng quy tắc hóa trị, xác định tỉ lệ
+ Xác định x, y (x, y thường là những số nguyên tố nhỏ nhất thỏa mãn tỉ lệ trên).
Ví dụ: Lập công thức hóa học của hợp chất được tạo bởi S hóa trị IV và O.
Hướng dẫn giải
+ Đặt công thức của hợp chất là SxOy.
+ Theo quy tắc hóa trị: x × IV = y × II
+ Ta có tỉ lệ:
+ Công thức hóa học của hợp chất là: SO2.
b) Xác định công thức hóa học của hợp chất khi biết phần trăm khối lượng của các nguyên tố và khối lượng phân tử của hợp chất
- Khi biết phần trăm khối lượng của hai nguyên tố A, B tạo nên hợp chất và khối lượng phân tử của chất đó, xác định công thức hóa học theo bước sau:
+ Đặt công thức hóa học của hợp chất AxBy.
+ Tính khối lượng của A, B trong một phân tử chất.
+ Tìm x, y.
Ví dụ: R là hợp chất của Fe và O, khối lượng phân tử của R là 72 amu. Biết phần trăm khối lượng của oxygen trong R là 22,22%. Hãy xác định công thức hóa học của R.
Hướng dẫn giải
+ Đặt công thức hóa học của R là FexOy.
+ Khối lượng của nguyên tố O trong một phân tử R là:
+ Khối lượng của nguyên tố S trong một phân tử R là:
72 – 16 = 56 (amu)
+ Ta có: 16 amu × y = 16 amu ⇒ y = 1
56 amu × x = 56 amu ⇒ x = 1
Vậy công thức hóa học của R là FeO.