Anonymous
0
0
Giải Hóa 11 trang 99 Kết nối tri thức
- asked 6 months agoVotes
0Answers
0Views
Giải Hóa 11 trang 99 Kết nối tri thức
Hoạt động 1 trang 99 Hóa học 11: Điều chế và thử tính chất hoá học của ethylene
Tiến hành:
- Cho vài viên đá bọt, 20 mL cồn 96° vào bình cầu. Rót 40 mL dung dịch H2SO4 đặc vào ống đong, sau đó rót từ từ H2SO4 đặc từ ống đong qua phễu vào bình cầu để tránh sự toả nhiệt quá mạnh.
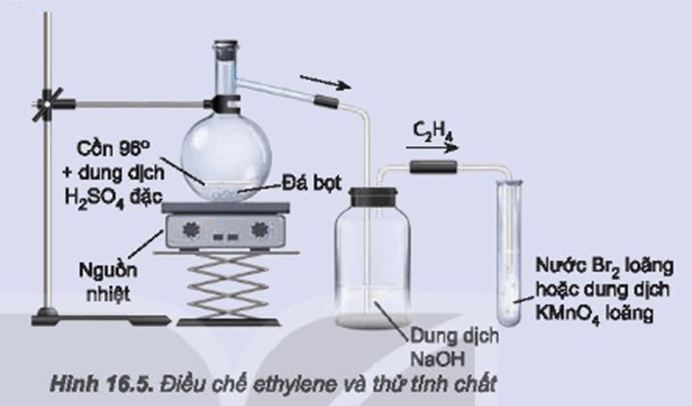
- Lắp bộ dụng cụ như Hình 16.5.
- Đun nóng đến khi ethylene sinh ra và sục ngay vào các ống nghiệm (1) và (2).
- Thay ống dẫn khí thuỷ tinh hình chữ L bằng ống dẫn thuỷ tinh có đầu vuốt nhọn.
Dùng que đóm đang cháy để đốt ethylene ở đầu ống dẫn khí.
Lưu ý: Dung dịch sulfuric acid đặc rơi vào da sẽ gây bỏng nặng, cần cẩn thận khi sử dụng.
Hãy giải thích hiện tượng và viết phương trình hoá học của phản ứng xảy ra.
Lời giải:
Đun cồn 96o với sulfuric acid đặc sinh ra khí ethylene (có lẫn tạp chất như CO2, SO2…).
Khí sinh ra được dẫn qua bình (1) để loại tạp chất; dẫn tiếp qua bình (2) thấy dung dịch Br2 (hoặc dung dịch KMnO4) nhạt dần đến mất màu do liên kết pi ở liên kết đôi của ethylene kém bền vững.
Đốt ethylene ở đầu ống dẫn khí, khí ethylene cháy và toả nhiều nhiệt.
Phương trình hoá học:
C2H5OH CH2 = CH2 + H2O
CH2 = CH2 + Br2 → CH2Br – CH2Br
3CH2 = CH2 + 2KMnO4 + 4H2O → 3HO – CH2 – CH2 – OH + 2MnO2 + 2KOH
C2H4 + 3O2 2CO2 + 2H2O.
Hoạt động 2 trang 99 Hóa học 11: Điều chế và thử tính chất hoá học của acetylene
Tiến hành:
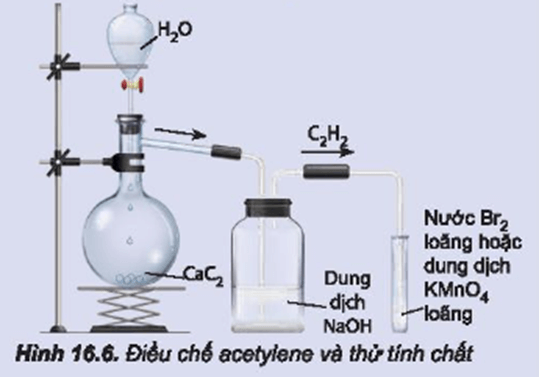
- Cho khoảng 5 g đất đèn vào bình cầu có nhánh và cho nước cất vào phễu nhỏ giọt. Lắp dụng cụ như Hình 16.6 (chú ý đuôi của phễu nhỏ giọt không chạm vào chất rắn).
- Mở khoá phễu nhỏ giọt để nước chảy từ từ xuống, khí acetylene sinh ra được sục ngay vào các ống nghiệm chứa dung dịch KMnO4 và nước Br2 đã chuẩn bị ở trên đến khi dung dịch mất màu.
- Thay ống dẫn khí thuỷ tinh hình chữ L bằng ống dẫn thuỷ tinh có đầu vuốt nhọn. Dùng que đóm đang cháy để đốt acetylene sinh ra ở đầu ống dẫn khí.
Hãy giải thích hiện tượng và viết phương trình hoá học của các phản ứng xảy ra.
Lời giải:
Đất đèn (thành phần chính CaC2) tác dụng với nước sinh ra khí acetylene (C2H2).
Khí này có thể lẫn tạp chất nên được dẫn qua bình (1) chứa NaOH để tinh chế.
Dẫn acetylene vào các ống nghiệm chứa dung dịch KMnO4 và nước Br2 thấy các dung dịch này nhạt dần đến mất màu do liên kết pi ở acetylene kém bền vững.
Khi đốt acetylene cháy, toả nhiều nhiệt.
Phương trình hoá học minh hoạ:
CaC2 + 2H2O → Ca(OH)2 + C2H2
CH ≡ CH + 2Br2 → CHBr2 – CHBr2
3CH ≡ CH + 8KMnO4 → 3KOOC – COOK + 8MnO2 + 2KOH + 2H2O