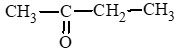Anonymous
0
0
Giải Hóa 11 Bài 23 (Kết nối tri thức): Hợp chất carbonyla
- asked 6 months agoVotes
0Answers
0Views
Giải Hóa 11 Bài 23: Hợp chất carbonyl
Mở đầu trang 136 Hóa học 11: Các aldehyde, ketone tạo nên mùi thơm đặc trưng của các loài động vật và thực vật. Nhiều aldehyde, ketone đóng vai trò quan trọng đối với cơ thể: tế bào võng mạc giúp mắt tiếp nhận ánh sáng được tạo thành từ aldehyde, các hormone giới tính nam và nữ là các ketone. Vậy, hợp chất carbonyl là gì và chúng có những tính chất nào?
Lời giải:
- Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có nhóm chức carbonyl (). Nhóm chức carbonyl có trong aldehyde, ketone …
- Hợp chất carbonyl có thể tham gia các phản ứng:
+ Phản ứng khử bởi các tác nhân khử như NaBH4; LiAlH4 …
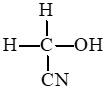
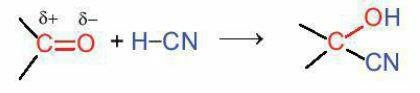
+ Phản ứng cộng HCN vào liên kết đôi C = O.
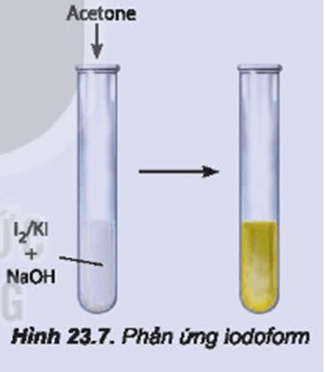
+ Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với I2 trong môi trường kiềm (phản ứng iodoform).
+ Aldehyde dễ bị oxi hoá bởi các tác nhân oxi hoá thông thường như: Br2/H2O; [Ag(NH3)2]OH, Cu(OH)2/OH−…
I. Khái niệm, danh pháp
Giải Hóa 11 trang 138
Câu hỏi 1 trang 138 Hóa học 11: Viết các công thức cấu tạo và gọi tên theo danh pháp thay thế của hợp chất carbonyl có công thức phân tử C4H8O.
Lời giải:
Các hợp chất carbonyl có công thức phân tử C4H8O:
- Hợp chất aldehyde:
CH3 – CH2 – CH2 – CHO: butanal;
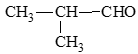
- Hợp chất ketone:
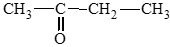
Câu hỏi 2 trang 138 Hóa học 11: Viết công thức cấu tạo của các hợp chất carbonyl có tên gọi dưới đây:
Lời giải:
a) propanal: CH3 – CH2 – CHO.
b) 3 – methylbut – 2 – enal:
c) pentan – 2 – one:
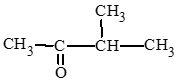
d) 3 – methylbutan – 2 – one.
Hoạt động trang 138 Hóa học 11: Cho biết các hợp chất dưới đây có khối lượng phân tử gần tương đương nhau và có nhiệt độ sôi như sau:
Lời giải:
- Các hợp chất carbonyl có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương. Do trong phân tử có chứa nhóm carbonyl phân cực làm cho phân tử hợp chất carbonyl phân cực.
- Các hợp chất carbonyl có nhiệt độ sôi thấp hơn các alcohol có khối lượng phân tử tương đương. Do các hợp chất carbonyl không tạo được liên kết hydrogen liên phân tử như alcohol.
III. Tính chất vật lí
Giải Hóa 11 trang 141
Giải Hóa 11 trang 142
Em có thể trang 144 Hóa học 11:
- Vận dụng các kiến thức về hợp chất carbonyl để giải thích: các ứng dụng của các aldehyde, ketone trong cuộc sống như quá trình sản xuất gương, làm dung môi,…
- Tìm hiểu về ứng dụng của các hợp chất aldehyde, ketone có trong tự nhiên và vai trò của một số aldehyde, ketone quan trọng trong cơ thể con người.
Lời giải:
- Phản ứng của aldehyde với thuốc thử Tollens tạo thành lớp bạc mỏng, sáng bóng bám vào thành bình phản ứng nên phản ứng này được ứng dụng trong quá trình sản xuất gương.
- Một số hợp chất carbonyl có thể hoà tan tốt nhiều chất hữu cơ khác nhau (kể cả các polymer) nên được ứng dụng để làm dung môi.
- Trong tự nhiên, các hợp chất chứa nhóm chức aldehyde và ketone tồn tại khá phổ biến trong tinh dầu của nhiều loài cây cỏ được sử dụng làm chất tạo hương trong công nghiệp thực phẩm và mĩ phẩm.
- Trong cơ thể người, một lượng nhỏ acetone được tạo ra qua quá trình chuyển hoá chất béo không hoàn toàn. Ở người khoẻ mạnh, acetone được hình thành ở gan và được chuyển hoá gần như hoàn toàn, chỉ có một lượng rất nhỏ xuất hiện ở nước tiểu. Sự hiện diện bất thường của acetone trong nước tiểu là một dấu hiệu của bệnh tiểu đường và được phát hiện qua việc xét nghiệm nước tiểu (chỉ số KET).
Lý thuyết Hợp chất carbonyl
1. Khái niệm, danh pháp
a. Khái niệm
b. Danh pháp
* Danh pháp thay thế:
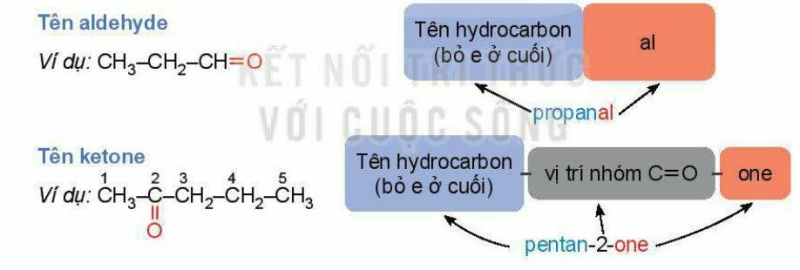
* Tên gọi thông thường:
Một số aldehyde, ketone đơn giản được gọi theo tên thông thường có nguồn gốc lịch sử. Tên thông thường của các aldehyde có nguồn gốc từ tên của acid tương ứng.
2. Đặc điểm cấu tạo
Liên kết đôi C=O phân cực về phía nguyên tử oxygen:
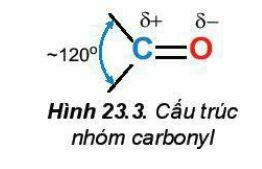
3. Tính chất vật lí
- Các aldehyde, ketone có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương.
- Ở nhiệt độ thường, các aldehyde ở thể khí và có phân tử khối nhỏ, tan tốt trong nước. Khi số nguyên tử carbon tăng thì độ tan của hợp chất carbonyl giảm dần.
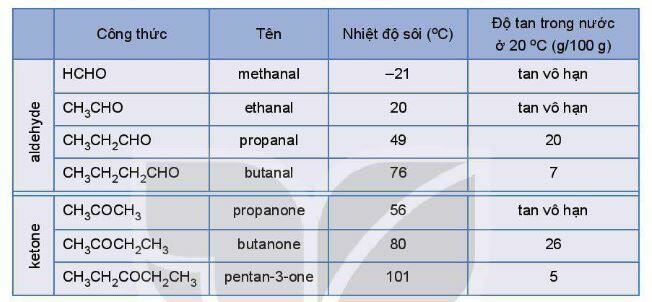
4. Tính chất hoá học
a. Phản ứng khử
b. Phản ứng oxi hóa aldehyde
* Oxi hóa aldehyde bởi nước:
Aldehyde bị oxi hoá bởi nước bromine tạo thành carboxylic acid.
Ví dụ: CH3CHO + Br2 + H2O → CH3COOH + 2HBr
* Oxi hoá aldehyde bởi thuốc thử Tollens
Thuốc thử Tollens là phức chất của ion Ag+ với ammonia, có công thức [Ag(NH3)2]OH. Ion Ag+ trong thuốc thử Tollens đóng vai trò là chất oxi hoá.
* Oxi hoá aldehyde bång copper(II) hydroxide
Aldehyde có thể bị oxi hoá bởi copper(II) hydroxide Cu(OH)2 trong môi trường kiềm khi đun nóng tạo thành kết tủa copper(I) oxide (Cu2O) màu đỏ gạch:
RCHO + 2 Cu(OH)2 + NaOH → RCOONa + Cu2O + 3H20
c. Phản ứng cộng
Hợp chất carbonyl có thể tham gia phản ứng cộng với HCN vào liên kết đối C=O.
d. Phản ứng tạo iodoform
Các hợp chất aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với I2, trong môi trường kiềm.

Phản ứng tạo sản phẩm kết tủa indoform nên phản ứng này được gọi là phản ứng lodoform và được dùng để nhận biết các aldehyde, ketone có nhóm methyl cạnh nhóm carbonyl.
5. Ứng dụng
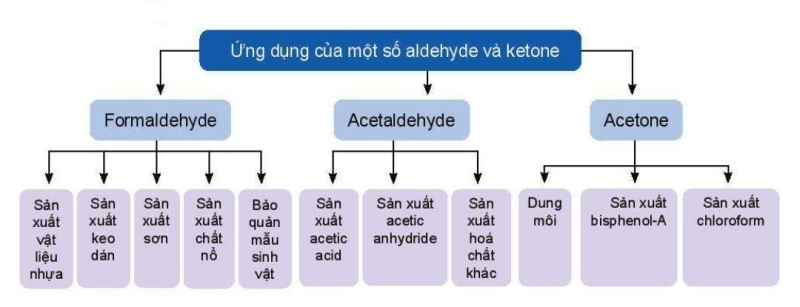
6. Điều chế
Một số hợp chất carbonyl được tổng hợp trong công nghiệp bằng phương pháp oxi hoá các hydrocarbon, oxi hóa ethylene thành acetaldehyde, oxi hoá cumene thành acetone.
Sơ đồ tư duy Hợp chất carbonyl
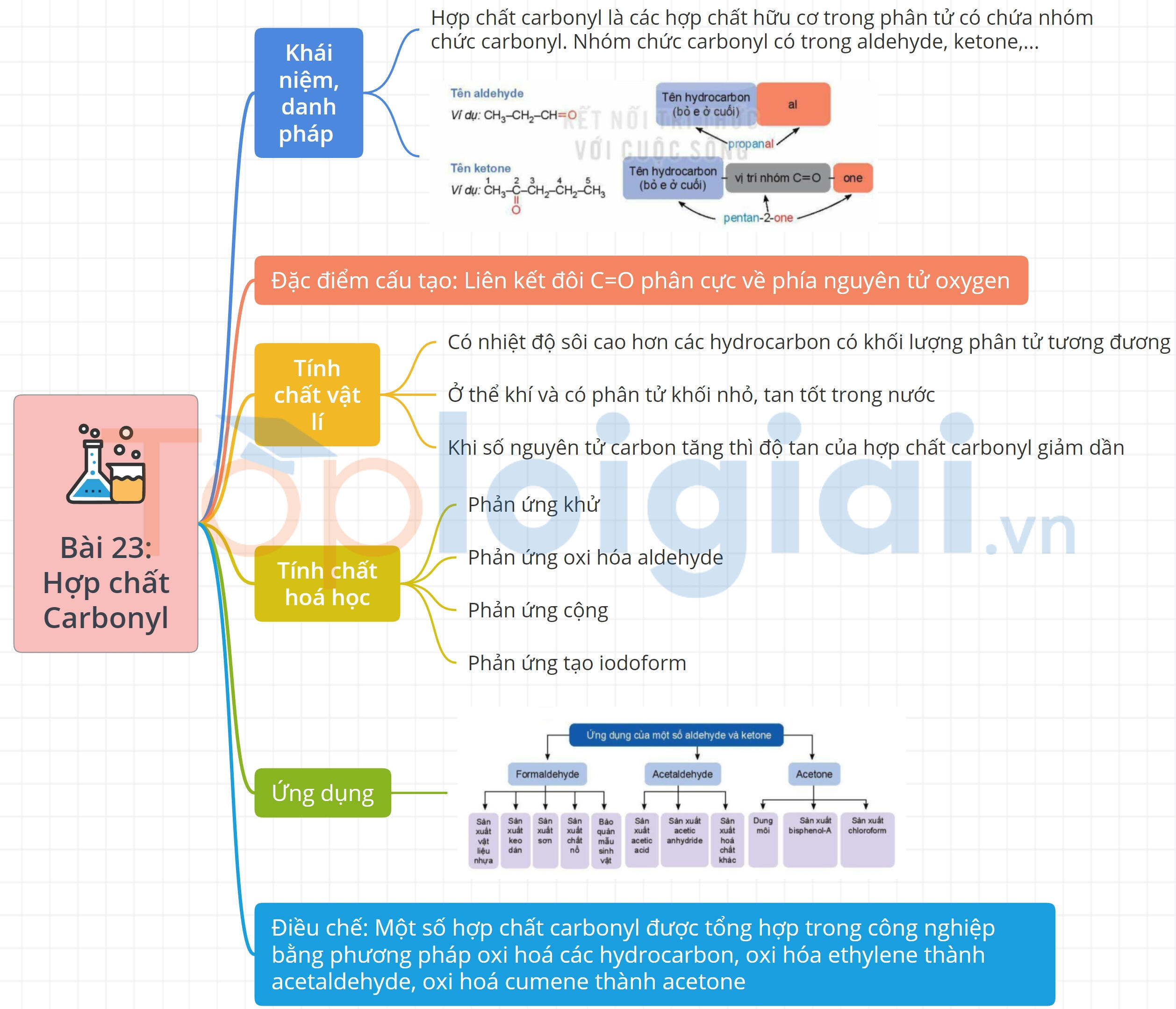
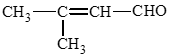
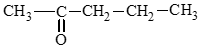
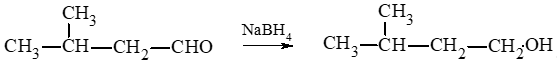 ;
;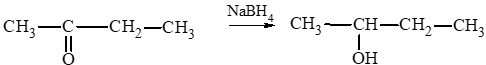 ;
;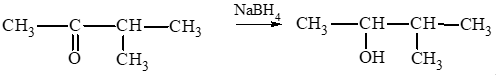 .
.