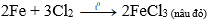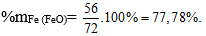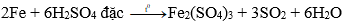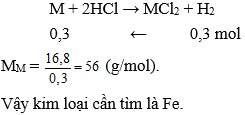Anonymous
0
0
TOP 40 câu Trắc nghiệm Sắt (có đáp án 2024) - Hóa học 9
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa học 9 Bài 19: Sắt
Bài giảng Hóa học 9 Bài 19: Sắt
Câu 1:
A. Dung dịch HCl.
B. Dung dịch H2SO4.
C. H2SO4 đặc, nóng.
D. H2SO4 đặc, nguội.
Đáp án: D
Sắt không phản ứng với H2SO4 đặc, nguội.
Câu 2:
A. H2SO4 đặc nóng, dư.
B. ZnSO4.
C. CuSO4.
D. HNO3 loãng, dư.
Đáp án: B
Giải thích:
Loại A vì:
![]()
Loại C vì:
Fe + CuSO4 → FeSO4 + Cu
Loại D vì:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Câu 3:
A. Màu trắng bạc, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt kém.
B. Màu trắng bạc, nặng, có ánh kim, dẫn điện và dẫn nhiệt tốt.
C. Màu trắng xám, nặng, có ánh kim, dẫn điện và dẫn nhiệt tốt.
D. Màu trắng xám, nhẹ, có ánh kim, dẫn điện và dẫn nhiệt tốt.
Đáp án: C
Giải thích: Sắt có màu trắng xám, nặng, có ánh kim, dẫn điện và dẫn nhiệt tốt.
Câu 4:
A. HCl.
B. NaOH.
C. H2SO4.
D. AgNO3.
Đáp án: B
Giải thích:
Để chuyển FeCl3 thành Fe(OH)3, người ta dùng dung dịch NaOH.
Phương trình hóa học:
FeCl3 + 3NaOHFe(OH)3↓ + 3NaCl
Câu 5:
Hiện tượng xảy ra là:
A. Không có hiện tượng gì cả.
B. Bạc được giải phóng, nhưng sắt không biến đổi.
C. Không có chất nào sinh ra, chỉ có sắt bị hoà tan.
D. Sắt bị hoà tan một phần, bạc được giải phóng.
Đáp án: D
Giải thích:
Do sắt đứng trước bạc trong dãy hoạt động hóa học nên khi ngâm một cây đinh sắt vào dung dịch bạc nitrat có phản ứng hóa học xảy ra như sau:
Fe + 2AgNO3 Fe(NO3)2 + 2Ag
Hiện tượng: Sắt bị hoà tan một phần, bạc được giải phóng.
Câu 6:
A. 3,25.
B. 2,80.
C. 5,08.
D. 6,5.
Đáp án: D
Giải thích:
2Fe + 3Cl2 2FeCl3
0,04 → 0,04mol
mmuối = 0,04. 162,5 = 6,5 gam
Câu 7:
A. Mg.
B. Zn.
C. Al.
D. Fe.
Đáp án: D
Giải thích:
Gọi kim loại là M.
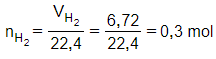
Phương trình hóa học:
M + 2HCl2MCl + H2
Theo phương trình:
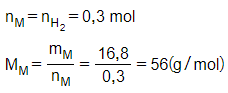
Vậy kim loại cần tìm là sắt (Fe).
Câu 8:
A. 858 kg.
B. 885 kg.
C. 588 kg.
D. 688 kg.
Đáp án: C
Giải thích:
Khối lượng Fe3O4 có trong 1 tấn quặng là:
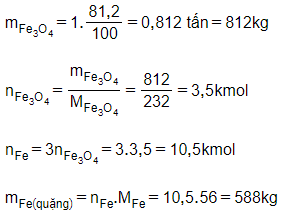
Câu 9:
A. Al.
B. Fe.
C. Cr.
D. Cu.
Đáp án: B
Giải thích:
Phương trình hóa học:
2A + 3Cl22ACl3
Bảo toàn khối lượng:
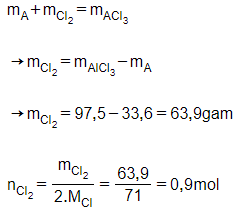
Theo phương trình:
Kim loại là sắt (Fe)
Câu 10:
A. Fe + 4HNO3Fe(NO3)3 + NO + 2H2O.
B. Fe + 6HNO3Fe(NO3)3 + 3NO + 3H2O.
C. Fe + 4HNO3Fe(NO3)3 + 2NO + 2H2O.
D. Fe + 8HNO3Fe(NO3)3 + 5NO + 4H2O.
Đáp án: A
Giải thích: Xét về cân bằng phương trình, phương trình nào cân bằng đúng là đúng.
Câu 11:
A. 17 gam.
B. 18 gam.
C. 19 gam.
D. 20 gam.
Đáp án: C
Giải thích:
Gọi số mol Fe tham gia phản ứng là x (mol). Ta có phương trình hóa học:
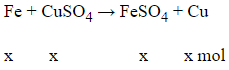
Bảo toàn khối lượng, ta có:
mthanh sắt tăng = mCu bám vào - mFe tan ra
(51 – 50) = 64x – 56x
→ x = 0,125 mol
Khối lượng muối sắt tạo thành là:
mmuối = 0,125.152 = 19 gam.
Câu 12:
A. FeO.
B. Fe2O3.
C. Fe3O4.
D. FeO và Fe2O3.
Đáp án: B
Giải thích:
Đặt oxit sắt cần tìm là FexOy.
Do oxit sắt phản ứng hoàn toàn với CO, nên 22,4 gam chất rắn thu được là Fe.
Ta có: nFe =
Bảo toàn khối lượng có:
mO (oxit) = moxit – mFe
= 32 – 22,4 = 9,6 gam.
→ x : y = nFe : nO (oxit)
= 0,4 : 0,6 = 2 : 3.
Vậy oxit sắt cần tìm là Fe2O3.
Câu 13:
A. 18,88 gam Fe và 4,32 gam Ag.
B. 18,78 gam Fe và 3,32 gam Ag.
C. 18,88 gam Fe và 3,32 gam Ag.
D. 18,78 gam Fe và 4,32 gam Ag.
Đáp án: A
Giải thích:
Giả sử số mol của AgNO3 là x mol.
Phương trình hóa học:
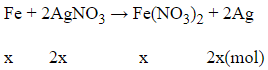
m tăng = 23,2 - 20 = 3,2 gam
mAg – mFe = 108.2x – 56.x = 3,2
x = 0,02 mol
m Fe còn lại = 20 - 0,02.56 = 18,88(g)
mAg = 0,04 . 108 = 4,32g
Câu 14:
FeFeCl3A BFe2(SO4)3DCFeO
Các chất A, B, C, D lần lượt là
A. FeS, Fe3O4, FeSO4, Fe2O3.
B. Fe(OH)3, Fe2O3, FeSO4, Fe(OH)2.
C. FeS, Fe2O3, FeSO4, Fe2O3.
D. FeS, FeO, Fe2O3,Fe(OH)3.
Đáp án: B
Giải thích:
Phương trình hóa học:
FeCl3 + 3NaOHFe(OH)3↓ (A) + 3NaCl
2Fe(OH)3 Fe2O3 (B) + 3H2O
FeO + H2SO4FeSO4 (C) + H2O
FeSO4 + 2NaOH → Fe(OH)2↓ (D) + Na2SO4
Câu 15:
A. FeO.
B. Fe2O3.
C. Fe3O4.
D. FeO Fe2O3.
Đáp án: A
Giải thích:
1mol Fe 1 mol oxit sắt
Công thức có chứa 1 nguyên tử Fe
Công thức oxit sắt là: FeO
Câu 16: Cho dây sắt quấn hình lò xo (đã được nung nóng đỏ) vào lọ đựng khí clo. Hiện tượng xảy ra là:
A. Sắt cháy tạo thành khói trắng dày đặt bám vào thành bình.
B. Không thấy hiện tượng phản ứng
C. Sắt cháy sáng tạo thành khói màu nâu đỏ
D. Sắt cháy sáng tạo thành khói màu đen
Đáp án: C
Giải thích:
Câu 17: Hoà tan hỗn hợp gồm Fe và Cu vào dung dịch HCl (vừa đủ). Các chất thu được sau phản ứng là:
A. FeCl2 và khí H2
B. FeCl2, Cu và khí H2
C. Cu và khí H2
D. FeCl2 và Cu
Đáp án: B
Giải thích:
Cu không phản ứng với HCl
Fe + 2HCl → FeCl2 + H2
Câu 18: Kim loại được dùng để làm sạch dung dịch FeSO4 có lẫn tạp chất là CuSO4 là
A. Fe
B. Zn
C. Cu
D. Al
Đáp án: A
Giải thích:
Sử dụng một lượng dư kim loại Fe
Fe + CuSO4 → FeSO4 + Cu
Lọc bỏ kim loại thu được dung dịch FeSO4 tinh khiết.
Câu 19: Trong các chất sau đây chất nào chứa hàm lượng sắt nhiều nhất?
A. FeS2
B. FeO
C. Fe2O3
D. Fe3O4
Đáp án: B
Giải thích:
Câu 20: Để chuyển FeCl3 thành Fe(OH)3, người ta dùng dung dịch:
A. HCl
B. H2SO4
C. NaOH
D. AgNO3
Đáp án: C
Giải thích:
FeCl3 + 3NaOH → Fe(OH)3 ↓ + 3NaCl
Câu 21: Phản ứng tạo ra muối sắt (III) sunfat là:
A. Sắt phản ứng với H2SO4 đặc, nóng.
B. Sắt phản ứng với dung dịch H2SO4 loãng
C. Sắt phản ứng với dung dịch CuSO4
D. Sắt phản ứng với dung dịch Al2(SO4)3
Đáp án: A
Giải thích:
Câu 22: Hoà tan 16,8g kim loại vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H2 (đktc). Kim loại đem hoà tan là (Biết trong muối thu được sau phản ứng kim loại có hóa trị II)
A. Mg
B. Zn
C. Pb
D. Fe
Đáp án: D
Giải thích:
Ta có: nkhí = 6,72 : 22,4 = 0,3 mol, gọi kim loại là M
Câu 23: Một tấn quặng manhetit chứa 81,2% Fe3O4. Khối lượng Fe có trong quặng là:
A. 858 kg
B. 885 kg
C. 588 kg
D. 724 kg
Đáp án: C
Giải thích:
Khối lượng Fe3O4 có trong 1 tấn quặng là:
Câu 24: Clo hoá 33,6g một kim loại A ở nhiệt độ cao thu được 97,5g muối ACl3. A là kim loại:
A. Al
B. Cr
C. Au
D. Fe
Đáp án: D
Giải thích:
2A + 3Cl2 → 2ACl3
Câu 25: Chất nào dưới đây không tác dụng với Fe?
A. HCl.
B. H2SO4 loãng.
C. H2SO4 đặc, nóng.
D. H2SO4 đặc, nguội.
Đáp án: D
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Hợp kim sắt: Gang, thép có đáp án
Trắc nghiệm Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn có đáp án
Trắc nghiệm Luyện tập chương 2: Kim loại có đáp án