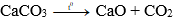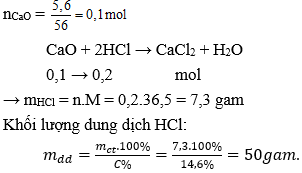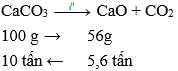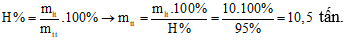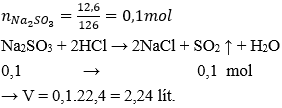Anonymous
0
0
TOP 40 câu Trắc nghiệm Một số oxit quan trọng (có đáp án 2024) – Hóa học 9
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa học 9 Bài 2: Một số oxit quan trọng
Bài giảng Hóa học 9 Bài 2: Một số oxit quan trọng (Phần A: Canxi oxit)
Bài giảng Hóa học 9 Bài 2: Một số oxit quan trọng (Phần B: Lưu huỳnh đioxit)
Câu 1:
A. Oxit bazơ
B. Oxit axit
C. Oxit trung tính
D. Oxit lưỡng tính
Đáp án: A
Giải thích: CaO là oxit bazơ.
Câu 2:
A. 0,25M
B. 0,45M
C. 0,50M
D. 0,75M
Đáp án: D
Giải thích:
200 ml = 0,2 lít
Số mol của SO2 là:
Phương trình phản ứng:
Theo phương trình phản ứng ta có số mol của là:
= 0,15 mol
Vậy nồng độ mol của H2SO3 là:
CM = = 0,75M.
Câu 3:
A. Tác dụng với oxit axit
B. Tác dụng với oxit bazơ
C. Tác dụng với axit
D. Tác dụng với bazơ
Đáp án: C
Giải thích: CaO dùng làm chất khử chua đất trồng là ứng dụng của tính chất hóa học là tác dụng với axit.
Câu 4:
A. KOH, CaO, H2O
B. CaO, NO2, BaCl2
C. NaOH, CaCl2, Na2SO4
D. KOH, NaCl, P2O5
Đáp án: A
Giải thích:
SO2 mang đầy đủ tính chất của một oxit axit.
SO2 phản ứng được với KOH, CaO, H2O.
Phương trình hóa học minh họa:
SO2 + 2KOH dư → K2SO3 + H2O
SO2 + CaO CaSO3
SO2 + H2O → H2SO3
Câu 5:
A. 16 gam
B. 17 gam
C. 18 gam
D. 19 gam
Đáp án: C
Giải thích:
Số mol của SO2 là:
= 0,15 mol
Số mol của CaO là:
nCaO = = 0,25 mol
Phương trình phản ứng:
SO2 + CaO → CaSO3
Ta có:
SO2 phản ứng hết
Theo phương trình phản ứng, ta có:
0,15 mol
Vậy khối lượng của CaSO3 là:
m = 0,15.120 = 18 gam.
Câu 6:
A. CaCO3 (r) → CaO (r) + CO2 (k)
B. Ca(OH)2 (dd) → CaO (r) + H2O (h)
C. CaSO4 (r) → CaO (r) + SO2 (k)
D. CaSO4 (r) → CaO (r) + SO2 (k)
Đáp án: A
Giải thích:
Phương trình hóa học dùng để điều chế CaO là:
CaCO3 (r) → CaO (r) + CO2 (k)
Câu 7:
A. 71 gam
B. 73 gam
C. 75 gam
D. 77 gam
Đáp án: B
Giải thích:
Số mol của CaO là:
nCaO = 0,2 mol
Phương trình phản ứng:
Theo phương trình phản ứng, ta có:
nHCl = 0,4 mol
Suy ra khối lượng của HCl là:
mHCl = 0,4.36,5 = 14,6 gam
Khối lượng dung dịch HCl đã dùng là:
mdd(HCl) = = 73 gam.
Câu 8:
A. Nước và quỳ tím
B. Dung dịch NaCl
C. Dung dịch KOH
D. Quỳ tím khô
Đáp án: A
Giải thích:
CaO là oxit bazơ tan trong nước tạo thành dung dịch bazơ, làm quỳ tím chuyển sang màu xanh.
CaO + H2O → Ca(OH)2
P2O5 là oxit axit tan trong nước tạo thành dung dịch axit, làm quỳ tím chuyển sang màu đỏ.
P2O5 + 3H2O → 2H3PO4
Câu 9:
A. CaSO3 và KCl
B. CaSO4 và HCl
C. CaSO3 và KOH
D. CaSO3 và HCl
Đáp án: D
Giải thích:
Phương trình phản ứng:
CaSO3 + 2HCl → CaCl2 + SO2 + H2O
Câu 10:
A. HCl
B. H2O, quỳ tím.
C. HNO3
D. không phân biệt được.
Đáp án: B
Giải thích:
- CaO + H2O → Ca(OH)2
Ca(OH)2 (dd) làm xanh quỳ tím.
- MgO không phản ứng với nước, không tan trong nước, không làm quỳ tím chuyển màu.
Câu 11:
A. 9,5 tấn
B. 10,5 tấn
C. 10 tấn
D. 9,0 tấn
Đáp án: B
Giải thích:
CaCO3 CaO + CO2
100 g → 56g
10 tấn ← 5,6 tấn
Do hiệu suất phản ứng là 95% nên lượng CaCO3 cần dùng là tấn.
Câu 12:
A. Khử chua cho đất
B. Khử độc môi trường
C. Sát trùng diệt nấm
D. Sản xuất cao su
Đáp án: D
Giải thích: Ứng dụng không phải của canxi oxit là sản xuất cao su.
Câu 13:
A. 0,448 lít
B. 0,224 lít
C. 0,112 lít
D. 0,336 lít
Đáp án: A
Giải thích:
Số mol của K2SO3 là:
= 0,02 mol
Phương trình phản ứng:
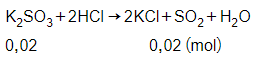
Theo phương trình phản ứng ta có:
= 0,02 mol
Vậy thể tích khí SO2 thu được ở đktc là:
V = 0,02.22,4 = 0,448 lít.
Câu 14:
A. O3
B. CO2
C. SO2
D. H2
Đáp án: C
Giải thích: Trong số các đáp án, chất chủ yếu gây nên mưa axit là: SO2.
Câu 15:
A. MgO
B. CuO
C. CaO
D. ZnO
Đáp án: C
Giải thích:
Trong phòng thí nghiệm, oxit được dùng làm chất hút ẩm (chất làm khô) là: CaO
Vì nó tác dụng với nước tạo thành Ca(OH)2
Phương trình phản ứng:
CaO + H2O → Ca(OH)2
Câu 16: Oxit được dùng làm chất hút ẩm (chất làm khô) trong phòng thí nghiệm là
A. CuO
B. ZnO
C. PbO
D. CaO
Đáp án: D
Câu 17: Sản phẩm của phản ứng phân hủy canxi cacbonat bởi nhiệt là:
A. CaO và CO
B. CaO và CO2
C. CaO và SO2
D. CaO và P2O5
Đáp án: B
Giải thích:
Câu 18: Để phân biệt 2 lọ mất nhãn đựng CaO và MgO ta dùng:
A. HCl
B. H2O, quỳ tím.
C. HNO3
D. không phân biệt được.
Đáp án: B
Giải thích:
CaO + H2O → Ca(OH)2
Ca(OH)2 (dd) làm xanh quỳ tím.
MgO không phản ứng với nước, không tan trong nước, không làm quỳ tím chuyển màu.
Câu 19: Cặp chất tác dụng với nhau sẽ tạo ra khí lưu huỳnh đioxit là
A. CaCO3 và HCl
B. Na2SO3 và H2SO4
C. CuCl2 và KOH
D. K2CO3 và HNO3
Đáp án: B
Giải thích:
Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
Câu 20: Chất nào sau đây góp phần nhiều nhất vào sự hình thành mưa axit ?
A. CO2
B. SO2
C. N2
D. O3
Đáp án: B
Câu 21: Dãy các chất tác dụng với lưu huỳnh đioxit là
A. Na2O, CO2, NaOH, Ca(OH)2
B. CaO, K2O, KOH, Ca(OH)2
C. HCl, Na2O, Fe2O3, Fe(OH)3
D. Na2O, CuO, SO3, CO2
Đáp án: B
Câu 22: Vôi sống có công thức hóa học là
A. Ca
B. Ca(OH)2
C. CaCO3
D. CaO
Đáp án: D
Câu 23: Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Khối lượng dung dịch HCl đã dùng là:
A. 50 gam
B. 40 gam
C. 60 gam
D. 73 gam
Đáp án: A
Giải thích:
Câu 24: Để thu được 5,6 tấn vôi sống với hiệu suất phản ứng đạt 95% thì lượng CaCO3 cần dùng là
A. 9,5 tấn
B. 10,5 tấn
C. 10 tấn
D. 9,0 tấn
Đáp án: B
Giải thích:
Do hiệu suất phản ứng là 95% nên lượng CaCO3 cần dùng là:
Câu 25: Hòa tan 12,6 gam natrisunfit vào dung dịch axit clohiđric dư. Thể tích khí SO2 thu được ở đktc là:
A. 2,24 lít
B. 3,36 lit
C. 1,12 lít
D. 4,48 lít
Đáp án: A
Giải thích:
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Tính chất hóa học của axit có đáp án
Trắc nghiệm Một số axit quan trọng có đáp án
Trắc nghiệm Luyện tập tính chất hóa học của oxit và axit có đáp án