Anonymous
0
0
TOP 40 câu Trắc nghiệm Hợp chất của cacbon (có đáp án 2023) – Hóa 11
- asked 6 months agoVotes
0Answers
0Views
Trắc nghiệm Hóa 11 Bài 16: Hợp chất của cacbon
Bài giảng Hóa 11 Bài 16: Hợp chất của cacbon
Câu 1:
A. 4,2g.
B. 5,8g.
C. 6,3g.
D. 6,5g.
Đáp án: C
Giải thích:
Gọi công thức chung của hai muối cacbonat là RCO3.
RCO3RO + CO2↑
→ Tạo muối axit, NaOH hết.
CO2+NaOH NaHCO3
→ nmuối = nNaOH = 0,075 mol
→ mmuối = 0,075.84 = 6,3 gam
Câu 2:
A. 5,91g.
B. 19,7g.
C. 78,8g.
D. 98,5g.
Đáp án: A
Giải thích:
→ Tạo hỗn hợp 2 muối.
Câu 3:
A. (NH4)3PO4.
B. NH4HCO3.
C. CaCO3.
D. NaCl.
Đáp án: B
Giải thích:
NH4HCO3NH3↑ + CO2↑ + H2O
Khi sử dụng bột nở này, khí NH3 và CO2 thoát ra làm cho bánh căng phồng và xốp.
Câu 4:
A. 4.
B. 5.
C. 6.
D. 7.
Đáp án: A
Giải thích:
Ca(HCO3)2CaCO3↓ + CO2 + H2O
→ Tổng các hệ số là 4.
Câu 5:
A. CaCO3, BaCO3.
B. Ca(HCO3)2, Ba(HCO3)2.
C. Na2CO3, K2CO3.
D. NaHCO3, KHCO3.
Đáp án: C
Giải thích: Muối cacbonat của kim loại kiềm bền với nhiệt.
Câu 6:
A. CO2.
B. N2.
C. CO.
D. CH4.
Đáp án: A
Giải thích:
Chất khí được tạo ra từ bình chữa cháy là CO2.
Thuốc giảm đau dạ dày là NaHCO3.
NaOH + CO2 → NaHCO3.
Câu 7:
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án: B
Giải thích:
Các chất thỏa mãn là CO2, NaHCO3 và NH4Cl.
CO2 + 2NaOH → Na2CO3 + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
NH4Cl + NaOH → NH3↑ + NaCl + H2O
Chú ý: SiO2 chỉ phản ứng với dung NaOH đặc nóng hoặc NaOH nóng chảy.
Câu 8:
A. 15,5g.
B. 26,5g.
C. 31g.
D. 46,5g.
Đáp án: D
Giải thích:
→ NaOH dư
→ Chất rắn gồm NaOH dư và muối Na2CO3.
Bảo toàn nguyên tố C:
Bảo toàn nguyên tố Na:
nNaOH dư = 1 – 0,25.2 = 0,5 mol
→ mchất rắn = 0,25.106 + 0,5.40 = 46,5 gam
Câu 9:
A. tăng 3,04g.
B. tăng 7,04g.
C. giảm 3,04g.
D. giảm 7,04g.
Đáp án: A
Giải thích:
→ Dung dịch Y chỉ có muối Ca(HCO3)2 và kết tủa X là CaCO3
→ Dung dịch sau phản ứng tăng 3,04 gam.
Câu 10:
A. Al2O3, Zn, Fe, Cu
B. Al2O3, ZnO, Fe, Cu
C. Al, Zn, Fe, Cu
D. Cu, Al, ZnO, Fe
Đáp án: A
Giải thích:
CO khử các oxit của kim loại sau Al trong dãy hoạt động hóa học.
→ Hỗn hợp rắn thu được gồm: Cu, Al2O3, Zn, Fe.
Câu 11:
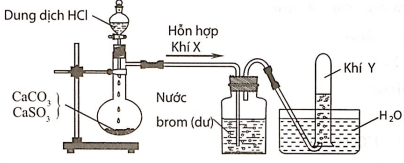
Khí Y là
A. CO2.
B. SO2.
C. H2.
D. Cl2.
Đáp án: A
Giải thích:
Hỗn hợp khí X gồm CO2 và SO2. Khí SO2 khi đi qua bình đựng nước brom đã bị giữ lại, còn khí Y thoát ra là CO2.
Câu 11:
A. có kết tủa, lượng kết tủa tăng dần, kết tủa không tan.
B. không có hiện tượng gì trong suốt quá trình thực hiện.
C. lúc đầu không thấy hiện tượng, sau đó có kết tủa xuất hiện.
D. có kết tủa, lượng kết tủa tăng dần, sau đó kết tủa tan.
Đáp án: D
Giải thích:
Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2 xảy ra phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Hiện tượng quan sát được: Dung dịch xuất hiện kết tủa trắng tăng dần đến cực đại, sau đó kết tủa tan dần đến hết.
Câu 12:
A. KCl.
B. KOH.
C. NaCl
D. K2CO3
Đáp án: D
Giải thích: Công thức của kali cacbonat là K2CO3.
Câu 13:
A. NaCl.
B. KNO3.
C. KCl.
D. HCl.
Đáp án: D
Giải thích:
HCl + NaHCO3 → CO2↑ + NaCl + H2O
Câu 14:
A. SO2 rắn.
B. CO2 rắn.
C. CO rắn.
D. H2O rắn.
Đáp án: B
Giải thích: Nước đá khô là CO2 rắn.
Câu 15:
A. 0,015.
B. 0,02.
C. 0,03.
D. 0,04.
Đáp án: B
Giải thích:
Nhận thấy:
→ Dung dịch Z chứa
Bảo toàn nguyên tố C:
Câu 16:
A. tăng 13,2g.
B. tăng 20g.
C. giảm 6,8g.
D. giảm 16,8g.
Đáp án: C
Giải thích:
Ta có:
→ Sau phản ứng thu được hai muối CaCO3 và Ca(HCO3)2
→ Khối lượng dung dịch sau phản ứng giảm 6,8 gam.
Câu 17:
A. 2,55.
B. 3,94.
C. 1,97.
D. 4,925.
Đáp án: B
Giải thích:
Câu 18:
A. 65,6.
B. 72,0.
C. 70,4.
D. 66,5.
Đáp án: C
Giải thích:
Sử dụng phương pháp đường chéo:
và nhỗn hợp khí = 0,5 mol
→
→ nO oxit =
→ mX = 64 + 0,4.16 = 70,4 gam
Câu 19:
A. 2,80.
B. 2,24.
C. 1,12.
D. 3,36.
Đáp án: B
Giải thích:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bảo toàn nguyên tố C ta có:
lít
Câu 20:
A.MgCl2.
B. Ca(OH)2.
C. Ca(HCO3)2.
D.NaOH.
Đáp án: B
Giải thích:
A và C không phản ứng → loại.
D. CO2 + 2NaOHdư → Na2CO3 + H2O → loại.
B. CO2 + Ca(OH)2 dư → CaCO3↓ + H2O
Câu 21:
A. 5 gam
B. 15 gam
C. 20gam
D. 40gam
Đáp án: C
Giải thích:
Theo bài → dung dịch X gồm các ion
→ dung dịch X
Bảo toàn điện tích →
Câu 22:
A. Quá trình đun nấu, đốt lò sưởi trong sinh hoạt.
B. Quá trình quang hợp của cây xanh.
C. Quá trình đốt nhiên liệu trong động cơ ô tô.
D. Quá trình đốt nhiên liệu trong lò cao.
Đáp án: B
Giải thích:
A. Khi đun nấu, đốt lò sưởi trong sinh hoạt sinh ra khí CO, CO2
→ gây ô nhiễm không khí
B. Quá trình quang hợp của cây xanh sinh ra khí oxi:
6CO2 + 6H2O >C6H12O6 + 6O2
→ không gây ô nhiễm không khí
C. Đốt nhiên liệu trong động cơ ô tô sinh ra khí SO2, H2S, CO2, NOx, …
→ gây ô nhiễm không khí
D. Đốt nhiên liệu trong lò cao sinh ra khí SO2, H2S, CO2, NOx,…
→ gây ô nhiễm không khí
Câu 23:
A. 9,68 gam.
B. 10,24 gam.
C. 9,86 gam.
D. 10,42 gam.
Đáp án: B
Giải thích:
Ta có: hỗn hợp khí Y gồm khí CO và CO2
→ mol
Bảo toàn khối lượng ta có:
mhỗn hợp chất rắn =
→ mX = 0,4.28 + 13,44 – 0,4.9.4 = 10,24 gam
Câu 24:
A. 0,75.
B. 1,5.
C. 2.
D. 2,5.
Đáp án: C
Giải thích:
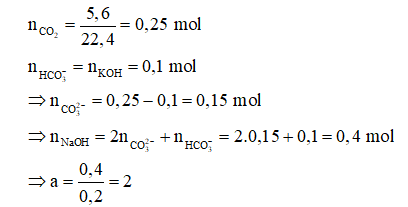
Câu 25:
A. CO2
B. CFC
C. SO2
D. NO2
Đáp án: A
Giải thích: CH4, CO2 là nguyên nhân gây ra hiệu ứng nhà kính.
Câu 26:
A. Cl2
B. CO
C. CO2
D. SO2,Cl2 và SO2
Đáp án: B
Giải thích:
CO là sản phẩm tạo thành khi đốt cháy than (C) trong điều kiện thiếu không khí. CO gây độc do nó cạnh tranh với nguyên tử oxi trong hồng cầu.
→ Khi hít phải 1 lượng lớn khí CO sẽ gây tử vong.
Câu 27:
A. đồng(II) oxit và mangan oxit.
B. đồng(II) oxit và than hoạt tính.
C. than hoạt tính.
D. đồng(II) oxit và magie oxit.
Đáp án: B
Giải thích:
- CuO loại bỏ CO bằng cách tác dụng trực tiếp CO:
CuO + CO → Cu + CO2
- Than hoạt tính loại bỏ CO bằng cách hấp thụ mạnh CO.
Câu 28:
A. đám cháy do xăng, dầu.
B. đám cháy nhà cửa, quần áo.
C. đám cháy do magie hoặc nhôm.
D. đám cháy do khí ga.
Đáp án: C
Giải thích:
Các kim loại mạnh như Mg, Al,..có thể cháy trong khí CO2
2Mg + CO22MgO + C
4Al + 3CO2 2Al2O3 + 3C
Do đó không dùng CO2 để dập tắt đám cháy do Mg, Al.
Câu 29:
A. Na2CO3.
B. NaHCO3.
C. MgCO3.
D. CaCO3.
Đáp án: A
Giải thích: Công thức của natri cacbonat là Na2CO3.
Câu 30:
A. CaO.
B. H2.
C. CO.
D. CO2.
Đáp án: D
Giải thích:
Khí X là CO2:
CaCO3CaO(rắn) + CO2 (khí)
Các câu hỏi trắc nghiệm Hóa lớp 11 có đáp án, chọn lọc khác:
Trắc nghiệm Silic và hợp chất của silic có đáp án
Trắc nghiệm Công nghiệp silicat có đáp án
Trắc nghiệm Luyện tập: Tính chất của cacbon, silic và các hợp chất của chúng có đáp án