Anonymous
0
0
Lý thuyết Phương trình hóa học (mới 2023 + Bài Tập) - Hóa học 8
- asked 6 months agoVotes
0Answers
0Views
Lý thuyết Hóa 8 Bài 16: Phương trình hóa học
Bài giảng Hóa 8 Bài 16: Phương trình hóa học
I. Lập phương trình hóa học
1. Phương trình hóa học
- Phương trình hóa học biểu diễn ngắn ngọn phản ứng hóa học.
- Ví dụ:
+ Phương trình chữ của phản ứng hóa học giữa khí hiđro và khí oxi tạo ra nước là:
Khí hiđro + khí oxi → nước
+ Thay tên các chất bằng công thức hóa học được sơ đồ của phản ứng:
H2 + O2 H2O
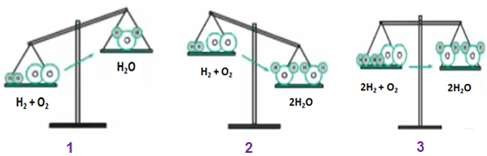
+ Ở hình 1: Nếu theo sơ đồ phản ứng: H2 + O2 H2O thì:
Vế trái có 2 nguyên tử H và 2 nguyên tử O
Vế phải có 2 nguyên tử H và 1 nguyên tử O
⇒ Vế trái có khối lượng lớn hơn vì hơn 1 nguyên tử O
+ Ở hình 2: Nếu vế trái nhiều hơn 1 nguyên tử O thì ta thêm hệ số 2 trước vế phải, lúc này:
Vế trái có 2 nguyên tử H và 2 nguyên tử O
Vế phải có 4 nguyên tử H và 2 nguyên tử O
⇒ Vế phải có khối lượng lớn hơn, do hơn 2 nguyên tử H
+ Ở hình 3: ta thêm hệ số 2 vào trước H2 và H2O
Vế trái có 4 nguyên tử H và 2 nguyên tử O
Vế phải có 4 nguyên tử H và 2 nguyên tử O
⇒ Khối lượng của 2 vế bằng nhau, số nguyên tử của mỗi nguyên tố đã bằng nhau
+ Phương trình hóa học của phản ứng viết như sau:
2H2 + O2 → 2H2O
2. Các bước lập phương trình hóa học
- Xét phản ứng giữa canxi với nước tạo thành canxi hiđroxit. Lập phương trình hóa học.
+ Bước 1: Viết sơ đồ phản ứng:
Ca + H2O Ca(OH)2 + H2
+ Bước 2: Cân bằng số nguyên tử mỗi nguyên tố
Bên phải số nguyên tử O là 2, nguyên tử H là 4, còn ở vế bên trái trong phân tử nước số nguyên tử O là 1, nguyên tử H là 2. Tức là số nguyên tử O, H ở vế phải gấp 2 lần vế trái
Do vậy cần thêm hệ số 2 vào trước phân tử nước ở vế trái.
Sau khi thêm hệ số ta thấy số nguyên tử Ca, O, H ở 2 vế bằng nhau.
+ Bước 3: Viết phương trình hóa học:
Ca + 2H2O → Ca(OH)2 + H2
Lưu ý:
- Hệ số viết cao bằng kí hiệu hóa học.
- Nếu trong công thức hóa học có nhóm nguyên tử thì coi cả nhóm như một đơn vị để cân bằng. Tức là, trước và sau phản ứng số nhóm nguyên tử phải bằng nhau.
II. Ý nghĩa của phương trình hóa học
- Phương trình hóa học cho biết tỉ lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng. Tỉ lệ này đúng bằng tỉ số hệ số các chất trong phương trình.
- Ví dụ: Xét phản ứng:
Ca + 2H2O → Ca(OH)2 + H2
Ta có, tỉ lệ số nguyên tử Ca : số phân tử H2O : số phân tử Ca(OH)2 : số phân tử H2 = 1 : 2 : 1 : 1.
Hiểu là cứ 1 nguyên tử Ca sẽ tác dụng với 2 phân tử H2O tạo ra 1 phân tử Ca(OH)2 và giải phóng 1 phân tử H2.
Trắc nghiệm Hóa học lớp 8 Bài 16: Phương trình hóa học
Câu 1:
A. Phương trình hóa học biểu diễn ngắn gọn phản ứng hóa học.
B. Lập phương trình hóa học bao gồm 4 bước cơ bản.
C. Phương trình hóa học luôn gồm 4 chất, trong đó có hai chất tham gia và hai chất sản phẩm.
D. Phương trình hóa học chỉ cho biết về kí hiệu các nguyên tố, chất tham gia phản ứng.
Câu 2:
A. Lập phương trình hóa học gồm có 3 bước cơ bản.
B. Phương trình hóa học biểu diễn ngắn gọn phản ứng hóa học
C. Sơ đồ phản ứng chính là phương trình hóa học.
D.Ý nghĩa của phương trình hóa học cho biết lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng cũng như giữa từng cặp chất trong phản ứng.
Câu3:
A. HCl
B. Cl2
C. H2
D. HO
Câu4:
Ba(OH)2+ CuSO4 → Cu(OH)2 + BaSO4
A. 1 : 1
B. 1 : 2
C. 2 : 1
D. 2 : 3
Câu 5:
A. 2H + O → H2O
B. H2 + O → H2O
C. H2 + O2→ 2H2O
D. 2H2 + O2→ 2H2O
Câu 6:
A. N + 3H → NH3
B. N2+ H2→ NH3
C. N2+ H2→2NH3
D. N2+ 3H2→ 2NH3
Câu 7:
A. C2H5OH + O2→ CO2+ H2O
B. C2H5OH + O2→ 2CO2+ H2O
C. C2H5OH + O2→ CO2+ 3H2O
D. C2H5OH + 3O2→ 2CO2+ 3H2O
Câu 8:
A. NH3+ O2→ NO + H2O
B. 2NH3+ O2→ 2NO + 3H2O
C. 4NH3+ O2→ 4NO + 6H2O
D. 4NH3+ 5O2→ 4NO + 6H2O
Câu 9:
A. 4P + 5O2→ 2P2O5
B. 2P + O2→ P2O5
C. 2P + 5O2→ 2P2O5
D. 2P + O2→ 2P2O5
Câu 10:
A. 2 mol O2phản ứng với 3 mol Fe
B. 1 mol Fe phản ứng với 1/2 mol O2
C. 1 mol Fe tạo ra 3 mol Fe3O4
D. 1 mol O2tạo ra 2 mol Fe3O4