Anonymous
0
0
Giải Hóa 10 Bài 3 ( Chân trời sáng tạo ): Nguyên tố hóa học
- asked 6 months agoVotes
0Answers
0Views
Giải bài tập Hóa lớp 10 Bài 3: Nguyên tố hóa học
Video giải Hóa lớp 10 Bài 3: Nguyên tố hóa học
Mở đầu trang 20 Hóa học 10: Kim cương và than chì có vẻ ngoài khác nhau. Tuy nhiên, chúng đều được tạo thành từ cùng một nguyên tố hóa học là nguyên tố carbon (C). Nguyên tố hóa học là gì? Một nguyên tử của nguyên tố hóa học có những đặc trưng cơ bản nào?
Lời giải:
- Nguyên tố hóa học là tập hợp những nguyên tử có cùng điện tích hạt nhân.
- Số đơn vị điện tích hạt nhân nguyên tử (còn gọi là số hiệu nguyên tử) của một nguyên tố hóa học và số khối được xem là những đặc trưng cơ bản của nguyên tử.
1. Hạt nhân nguyên tử
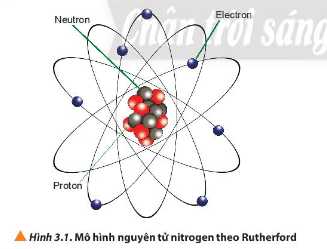
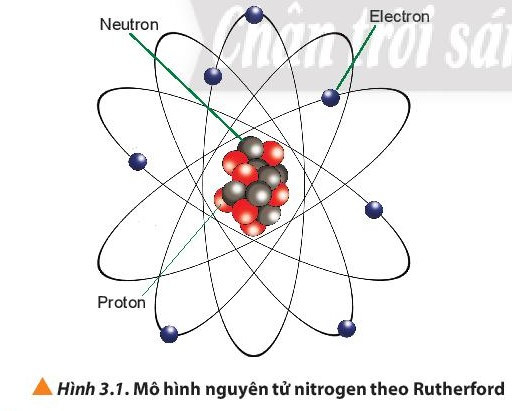
Câu hỏi 1 trang 20 Hóa học 10: Quan sát Hình 3.1, cho biết nguyên tử nitrogen có bao nhiêu proton, neutron và electron.
Lời giải:
Dựa vào hình 3.1 ta thấy: Nguyên tử nitrogen có 7 proton, 7 neutron và 7 electron.
Câu hỏi 2 trang 20 Hóa học 10: Điện tích hạt nhân của nguyên tử nitrogen có giá trị là bao nhiêu?
Lời giải:
Nguyên tử nitrogen có số đơn vị điện tích hạt nhân Z = số proton = 7.
Điện tích hạt nhân của nguyên tử nitrogen bằng +Z = +7.
Luyện tập trang 20 Hóa học 10: Nguyên tử sodium có 11 proton. Cho biết số đơn vị điện tích hạt nhân và số electron của nguyên tử này.
Lời giải:
Nguyên tử sodium có số đơn vị điện tích hạt nhân (Z) = số proton = số electron = 11.
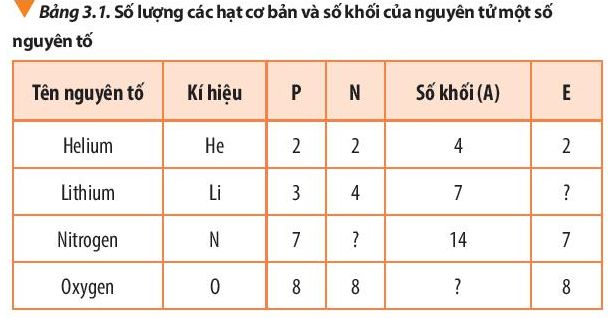
Câu hỏi 3 trang 21 Hóa học 10: Bổ sung những dữ liệu còn thiếu trong bảng 3.1.
Lời giải:
Vận dụng:
Số khối (A) = số proton (P) + số neutron (N)
Số proton (P) = số electron (E)
Tên nguyên tố |
Kí hiệu |
P |
N |
Số khối (A) |
E |
|
Helium |
He |
2 |
2 |
4 |
2 |
|
Lithium |
Li |
3 |
4 |
7 |
3 |
|
Nitrogen |
N |
7 |
7 |
14 |
7 |
|
Oxygen |
O |
8 |
8 |
16 |
8 |
2. Nguyên tố hóa học
Câu hỏi 4 trang 21 Hóa học 10: Nguyên tố carbon có số hiệu nguyên tử là 6. Xác định điện tích hạt nhân của nguyên tử này.
Lời giải:
Điện tích hạt nhân của carbon (+Z) là +6.
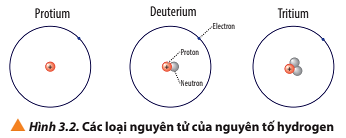
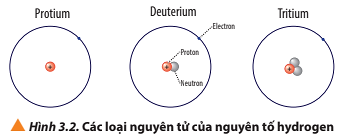
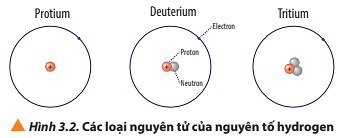
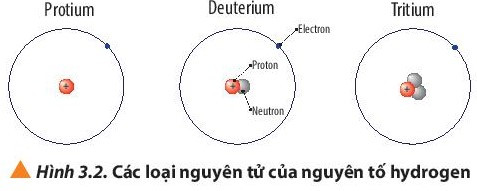
Câu hỏi 5 trang 22 Hóa học 10: Quan sát Hình 3.2, cho biết số proton, số neutron, số electron và điện tích hạt nhân của từng loại nguyên tử của nguyên tố hydrogen.
Lời giải:
Nguyên tử |
Số proton |
Số neutron |
Số electron |
Điện tích hạt nhân |
|
Protium |
1 |
0 |
1 |
+1 |
|
Deuterium |
1 |
1 |
1 |
+1 |
|
Tritium |
1 |
2 |
1 |
+1 |
Câu hỏi 6 trang 22 Hóa học 10: Kí hiệu nguyên tử cho biết những thông tin nào?
Lời giải:
Kí hiệu nguyên tử cho biết:
- Kí hiệu nguyên tố hóa học (X)
- Số khối (A)
- Số hiệu nguyên tử (Z)
Ví dụ:

Luyện tập trang 22 Hóa học 10: a) Viết kí hiệu các nguyên tử của nguyên tố hydrogen (Hình 3.2).
Lời giải:
a)
- Nguyên tử protium: 1 proton, 0 neutron ⇒ Z = 1, A = 1.
Kí hiệu: .
- Nguyên tử deuterium: 1 proton, 1 neutron ⇒ Z = 1, A = 2.
Kí hiệu: .
- Nguyên tử tritium: 1 proton, 2 neutron ⇒ Z = 1, A = 3.
Kí hiệu:
b)
- Nguyên tử oxygen có 8 electron, 8 neutron.
+ Số E = Số P = Z = 8
+ Số khối A = P + N = 8 + 8 = 16
⇒ Kí hiệu nguyên tử: .
3. Đồng vị
Câu hỏi 7 trang 22 Hóa học 10: Quan sát Hình 3.2, so sánh điểm giống và khác nhau giữa các loại nguyên tử của nguyên tố hydrogen.
Lời giải:
Các loại nguyên tử của nguyên tố hydrogen, có các điểm:
+ Giống nhau: đều có 1 proton và 1 electron;
+ Khác nhau: số lượng hạt neutron (protium không có neutron; deuterium có 1 neutron; tritium có 2 neutron).
Luyện tập trang 23 Hóa học 10: Kim cương là một trong những dạng tồn tại của nguyên tố carbon trong tự nhiên. Nguyên tố này có hai đồng vị bền với số khối lần lượt là 12 và 13. Hãy viết kí hiệu nguyên tử của hai đồng vị này.
Lời giải:
- Carbon có 6 proton ⇒ Số hiệu nguyên tử Z = 6.
- Kí hiệu nguyên tử carbon có số khối bằng 12 là: ;
- Kí hiệu nguyên tử carbon có số khối bằng 13 là: ;
4. Nguyên tử khối và nguyên tử khối trung bình
Câu hỏi 8 trang 23 Hóa học 10: Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron. Nguyên tử khối của Mg là bao nhiêu?
Lời giải:
Một cách gần đúng có thể coi nguyên tử khối có giá trị bằng số khối.
⇒ Nguyên tử khối của Mg = số khối (A) = số proton + số neutron = 24 (amu)
Câu hỏi 9 trang 23 Hóa học 10: Trong tự nhiên, nguyên tố copper có hai đồng vị với phần trăm số nguyên tử tương ứng là (69,15%) và (30,85%). Hãy tính nguyên tử khối trung bình của nguyên tố copper.
Lời giải:
Nguyên tử khối trung bình của nguyên tố copper:
.
Vận dụng trang 24 Hóa học 10: Trong thể dục thể thao, có một số vận động viên sử dụng các loại chất kích thích trong thi đấu, gọi là doping, dẫn đến thành tích đạt được của họ không thật so với năng lực vốn có. Một trong các loại doping thường gặp nhất là testosterone tổng hợp.
Lời giải:
Tỉ lệ hai đồng vị (98,98%) và (1,11%) trong testosterone tự nhiên trong cơ thể là
Đối với kết quả mẫu phân tích ta có:
⇒ > 89, 171
⇒ Từ kết quả thu được, em nghi ngờ vận động viên này đã có sử dụng doping.
Bài tập (trang 25)
Bài 1 trang 25 Hóa học 10: Một nguyên tử X gồm 16 proton, 16 electron và 16 neutron. Nguyên tử X có kí hiệu là:
Lời giải:
Đáp án: C
- Nguyên tử X có 16 proton ⇒ X là sulfur (S), loại đáp án B.
- Số hiệu nguyên tử (Z) = số proton = 16.
- Số khối (A) = số proton + số neutron = 16 + 16 = 32.
⇒ Kí hiệu nguyên tử X: .
Bài 2 trang 25 Hóa học 10: Silicon là nguyên tố được sử dụng để chế tạo vật liệu bán dẫn, có vai trò quan trọng trong sản xuất công nghiệp. Trong tự nhiên, nguyên tố này có 3 đồng vị với số khối lần lượt là 28, 29, 30. Viết kí hiệu nguyên tử cho mỗi đồng vị của silicon. Biết nguyên tố silicon có số hiệu nguyên tử là 14.
Lời giải:
Kí hiệu nguyên tử của các đồng vị silicon là: , và .
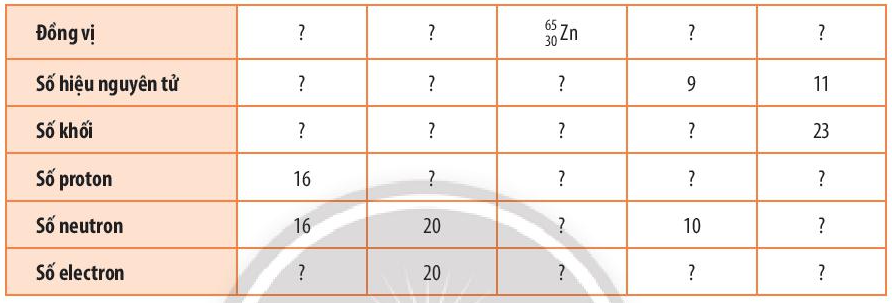
Bài 3 trang 25 Hóa học 10: Hoàn thành những thông tin chưa biết trong bảng sau:
Lời giải:
Đồng vị |
|
|
|
|
|
Số hiệu nguyên tử |
16 |
20 |
30 |
9 |
11 |
Số khối |
32 |
40 |
65 |
19 |
23 |
Số proton |
16 |
20 |
30 |
9 |
11 |
Số neutron |
16 |
20 |
35 |
10 |
12 |
Số electron |
16 |
20 |
30 |
9 |
11 |
Bài 4 trang 25 Hóa học 10: Trong tự nhiên, magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg. Phương pháp phổ khối lượng xác nhận đồng vị 26Mg chiếm tỉ lệ phần trăm số nguyên tử là 11%. Biết rằng nguyên tử khối trung bình của Mg là 24,32. Tính % số nguyên tử của đồng vị 24Mg, đồng vị 25Mg?
Lời giải:
Gọi % số nguyên tử của mỗi đồng vị 24Mg, 25Mg lần lượt là x, y.
Theo bài ta có hệ phương trình sau:
1. Hạt nhân nguyên tử
- Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E).
- Điện tích hạt nhân = + Z.
- Số khối (A) = số proton (P) + số neutron (N)
Ví dụ: Nguyên tử aluminium (Al) có 13 proton, 14 neutron. Suy ra:
+ Nguyên tử aluminium có số đơn vị điện tích hạt nhân = số proton = số electron = 13.
+ Điện tích hạt nhân nguyên tử aluminium là +13.
+ Số khối A = số proton (P) + số neutron (N) = 13 + 14 = 27.
II. Nguyên tố hóa học
1. Số hiệu nguyên tử
- Số đơn vị điện tích hạt nhân nguyên tử của một nguyên tố được gọi là số hiệu nguyên tử (Z) của nguyên tố đó.
- Mỗi nguyên tố hóa học có một số hiệu nguyên tử.
- Số hiệu nguyên tử (kí hiệu là Z) cho biết:
+ Số proton trong hạt nhân nguyên tử.
+ Số electron trong nguyên tử.
Ví dụ: Nguyên tố carbon có số hiệu nguyên tử là 6. Suy ra:
+ Số proton trong hạt nhân nguyên tử carbon = 6
+ Số electron trong nguyên tử carbon = 6
2. Nguyên tố hóa học
- Nguyên tố hóa học là tập hợp những nguyên tử có cùng điện tích hạt nhân.
Ví dụ: Protium; deuterium và tritium là các loại nguyên tử của nguyên tố hydrogen.
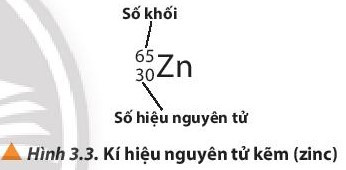
3. Kí hiệu nguyên tử
- Số đơn vị điện tích hạt nhân nguyên tử (số hiệu nguyên tử) của một nguyên tố hóa học và số khối được xem là những đặc trưng cơ bản của nguyên tử.
- Để kí hiệu nguyên tử, người ta thường ghi các chỉ số đặc trưng ở bên trái kí hiệu nguyên tố với số khối A ở phía trên, số hiệu nguyên tử Z ở phía dưới.

Ví dụ:
III. Đồng vị
- Các đồng vị của một nguyên tố hóa học là những nguyên tử có cùng số proton (P), cùng số hiệu nguyên tử (Z), nhưng khác nhau về số neutron (N). Do đó, số khối (A) của chúng khác nhau.
- Ví dụ: Potassium (K) có 3 đồng vị là:
- Trong tự nhiên, hầu hết các nguyên tố được tìm thấy dưới dạng hỗn hợp của các đồng vị.
- Ngoài các đồng vị bền, các nguyên tố hóa học còn có một số đồng vị không bền, gọi là các đồng vị phóng xạ, được sử dụng nhiều trong đời sống, y học, nghiên cứu khoa học…
IV. Nguyên tử khối và nguyên tử khối trung bình
1. Nguyên tử khối
- Nguyên tử khối là khối lượng tương đối của nguyên tử.
- Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử (1 amu).
- Một cách gần đúng, coi nguyên tử khối có giá trị bằng số khối.
Ví dụ: Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron.
⇒ Nguyên tử khối của Mg = 12 + 12 = 24 amu
2. Nguyên tử khối trung bình
- Mỗi nguyên tố thường có nhiều đồng vị, do đó trong thực tế người ta thường sử dụng giá trị nguyên tử khối trung bình.
- Muốn xác định giá trị nguyên tử khối trung bình của một nguyên tố, ta cần phải biết được phần trăm số nguyên tử các đồng vị của nguyên tố đó trong tự nhiên. Người ta thường dùng phương pháp phổ khối lượng để xác định phần trăm số nguyên tử các đồng vị tự nhiên của các nguyên tố.
Trong đó:
: là nguyên tử khối trung bình của X
Ai: là nguyên tử khối đồng vị thứ i
ai: là tỉ lệ % số nguyên tử đồng vị thứ i
Ví dụ:
Trong tự nhiên, nguyên tố copper có hai đồng vị với phần trăm số nguyên tử tương ứng là (69,15%) và (30,85%). Nguyên tử khối trung bình của nguyên tố copper là: