Anonymous
0
0
Nhôm(III) oxit tác dụng với axit sunfuric theo phương trình phản ứng
- asked 6 months agoVotes
0Answers
0Views
Giải Hóa 8 Bài 38: Bài luyện tập 7
Video Giải Bài 5 trang 132 Hóa học lớp 8
Bài 5 trang 132 Hóa học lớp 8:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tính lượng muối nhôm sunfat được tạo thành nếu đã sử dụng 49 gam axit sunfuric nguyên chất tác dụng với 60 gam nhôm oxit. Sau phản ứng chất nào còn dư ? Lượng dư của chất đó là bao nhiêu ?
Lời giải:
= 49 : 98 = 0,5 mol
= 60 : 102 = 0,59 mol
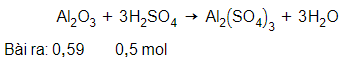
So sánh tỉ lệ → Vậy Al2O3 dư, H2SO4 hết. Số mol sản phẩm thu được tính theo số mol H2SO4.
Theo phương trình hóa học ta có: