Anonymous
0
0
Giải bài tập trang 25 Chuyên đề Hóa 10 Bài 3 - Cánh diều
- asked 6 months agoVotes
0Answers
0Views
Giải bài tập trang 25 Chuyên đề Hóa 10 - Cánh diều
Luyện tập 2 trang 25 Chuyên đề Hóa 10:Nếu ở ví dụ 2, Ea = 50 kJ mol-1thì tốc độ phản ứng thay đổi như thế nào?
Trả lời:
Thay Ea = 50 kJ mol-1 ; T1 = 298; T2 = 308 vào phương trình (7) ta có:
≈ 1,93
Vậy trong trường hợp Ea = 50 kJ mol-1thì tốc độ phản ứng tăng khoảng 1,93 lần.
Vận dụng 2 trang 25 Chuyên đề Hóa 10: Hãy liên hệ kết quả ở ví dụ 2 với hệ số Van’t Hoff về sự thay đổi tốc độ phản ứng theo nhiệt độ
Trả lời:
Theo Van’t Hoff với đa số các phản ứng, khi nhiệt độ tăng 10oC thì tốc độ phản ứng tăng từ 2 – 4 lần. Hệ số nhiệt độ Van’t Hoff là γ = 2 – 4
Kết quả ở ví dụ 2 phù hợp với hệ số Van’t Hoff về sự thay đổi tốc độ phản ứng theo nhiệt độ
3. Vai trò của chất xúc tác
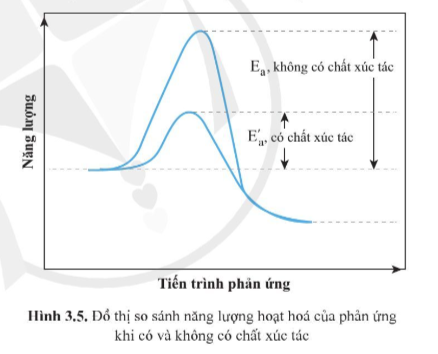
Câu hỏi 3 trang 25 Chuyên đề Hóa 10: Một phản ứng diễn ra ở một nhiệt độ không đổi, khi thêm chất xúc tác, tốc độ phản ứng tăng lên do năng lượng hoạt hóa bị thay đổi. Vậy chất xúc tác làm tăng hay giảm năng lượng hoạt hóa của phản ứng?
Trả lời:
Đối với một phản ứng, năng lượng hoạt hóa Ea càng nhỏ thì tốc độ phản ứng càng cao.
Chất xúc tác làm tăng tốc độ phản ứng ⇒ Chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng.
Chú ý:
Thực tế các nghiên cứu đã chỉ ra chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng.